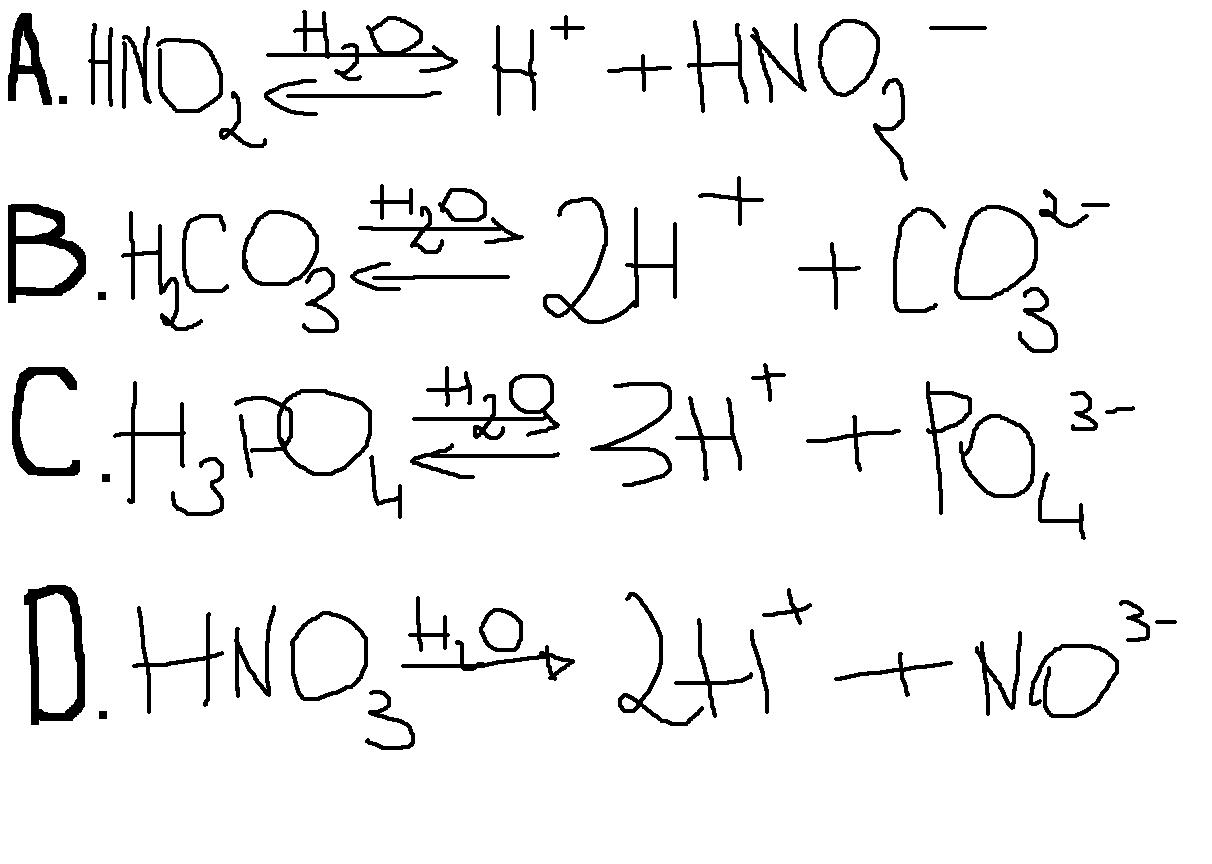Cześć! Dzisiaj zajmiemy się dysocjacją kwasu azotowego(V), a konkretnie tym, jak poprawnie zapisać równanie reakcji. To może brzmieć skomplikowanie, ale obiecuję, że rozłożymy to na czynniki pierwsze i wszystko stanie się jasne.
Co to jest Dysocjacja?
Zacznijmy od podstaw. Dysocjacja to po prostu rozpad pewnej substancji na mniejsze części – jony. Wyobraź sobie, że masz klocki LEGO połączone w jedną całość. Dysocjacja to jakby te klocki się rozłączyły. W chemii najczęściej mówimy o dysocjacji w wodzie, bo woda jest świetnym rozpuszczalnikiem.
Żeby to lepiej zrozumieć, pomyśl o soli kuchennej, czyli chlorku sodu (NaCl). Kiedy wrzucisz sól do wody, ona się rozpuszcza, prawda? Ale tak naprawdę, sól nie tylko „znika”, ale rozpada się na jony sodu (Na+) i jony chlorkowe (Cl-). To właśnie jest dysocjacja jonowa.
Jony to atomy lub grupy atomów, które mają ładunek elektryczny. Kationy to jony z ładunkiem dodatnim (utraciły elektron/elektrony), a aniony to jony z ładunkiem ujemnym (zyskały elektron/elektrony). W przykładzie z solą, jon sodu (Na+) jest kationem, a jon chlorkowy (Cl-) jest anionem.
Kwasy i Ich Dysocjacja
Kwasy to substancje, które w roztworze wodnym oddają jony wodorowe (H+). To właśnie obecność jonów wodorowych sprawia, że roztwór ma właściwości kwasowe. Im więcej jonów wodorowych, tym roztwór jest bardziej kwaśny. Pomyśl o soku z cytryny – jest kwaśny, bo zawiera kwas cytrynowy, który dysocjuje w wodzie, uwalniając jony wodorowe.
Dysocjację kwasów możemy zapisać za pomocą równań chemicznych. Takie równanie pokazuje, jak cząsteczka kwasu rozpada się na jony w wodzie.
Kwas Azotowy(V) (HNO3)
Teraz skupimy się na kwasie azotowym(V), którego wzór to HNO3. Jest to silny kwas, co oznacza, że w wodzie dysocjuje niemal całkowicie. Co to znaczy "niemal całkowicie"? To znaczy, że prawie wszystkie cząsteczki kwasu rozpadają się na jony.
Kwas azotowy(V) jest używany w wielu dziedzinach, np. do produkcji nawozów sztucznych, materiałów wybuchowych i w laboratoriach chemicznych. Jest to kwas bardzo żrący, więc należy z nim pracować ostrożnie!
Równanie Dysocjacji Kwasu Azotowego(V)
Jak zatem poprawnie zapisać równanie dysocjacji kwasu azotowego(V)? Oto ono:
HNO3 → H+ + NO3-
Wyjaśnijmy, co tu się dzieje:
- HNO3 to cząsteczka kwasu azotowego(V).
- → (strzałka) oznacza, że zachodzi reakcja dysocjacji.
- H+ to jon wodorowy (kation), który nadaje właściwości kwasowe.
- NO3- to jon azotanowy(V) (anion).
Zauważ, że cząsteczka kwasu azotowego(V) rozpada się na dwa jony: jon wodorowy (H+) i jon azotanowy(V) (NO3-). Ważne jest, aby pamiętać o znakach ładunków jonów. Jon wodorowy ma ładunek +1, a jon azotanowy(V) ma ładunek -1. Suma ładunków po obu stronach równania musi być równa zero (cząsteczka HNO3 jest obojętna).
Dlaczego Ważne Jest Poprawne Zapisywanie Równań?
Poprawne zapisywanie równań chemicznych jest bardzo ważne, ponieważ pozwala nam zrozumieć, co się dzieje podczas reakcji chemicznej. Błędy w zapisie mogą prowadzić do błędnych wniosków na temat przebiegu reakcji i jej efektów. Ponadto, poprawne równania są niezbędne do przeprowadzania obliczeń stechiometrycznych, czyli obliczeń dotyczących ilości reagentów i produktów w reakcji chemicznej.
Podsumowanie
Podsumowując, dysocjacja to rozpad substancji na jony w roztworze, najczęściej wodnym. Kwasy dysocjują, oddając jony wodorowe (H+). Kwas azotowy(V) (HNO3) jest silnym kwasem, który dysocjuje niemal całkowicie na jony wodorowe (H+) i jony azotanowe(V) (NO3-). Poprawne równanie dysocjacji kwasu azotowego(V) to: HNO3 → H+ + NO3-.
Mam nadzieję, że teraz temat dysocjacji kwasu azotowego(V) jest dla Ciebie bardziej zrozumiały. Pamiętaj, że kluczem do sukcesu jest zrozumienie podstawowych definicji i konceptów. Powodzenia w dalszej nauce chemii!
Jeśli nadal masz pytania, nie wahaj się szukać więcej informacji lub poprosić o pomoc nauczyciela lub kolegów. Nauka chemii może być fascynująca, jeśli podejdzie się do niej z ciekawością i chęcią zrozumienia.