Kwas węglowy, czyli H2CO3, to jeden z najważniejszych kwasów nieorganicznych. Powstaje w wyniku reakcji dwutlenku węgla (CO2) z wodą (H2O). Jego struktura, choć prosta, ma ogromne znaczenie w wielu procesach chemicznych i biologicznych.
Podstawowe informacje o kwasie węglowym
Kwas węglowy jest kwasem słabym. Oznacza to, że w roztworze wodnym ulega jedynie częściowej dysocjacji. W przeciwieństwie do mocnych kwasów, takich jak kwas solny, nie dysocjuje w całości na jony.
Jego powstawanie jest reakcją odwracalną. Równowaga tej reakcji jest silnie przesunięta w stronę dwutlenku węgla i wody. Dlatego też, stężenie kwasu węglowego w roztworach wodnych jest zazwyczaj bardzo niskie. To czyni go nietrwałym w czystej postaci.
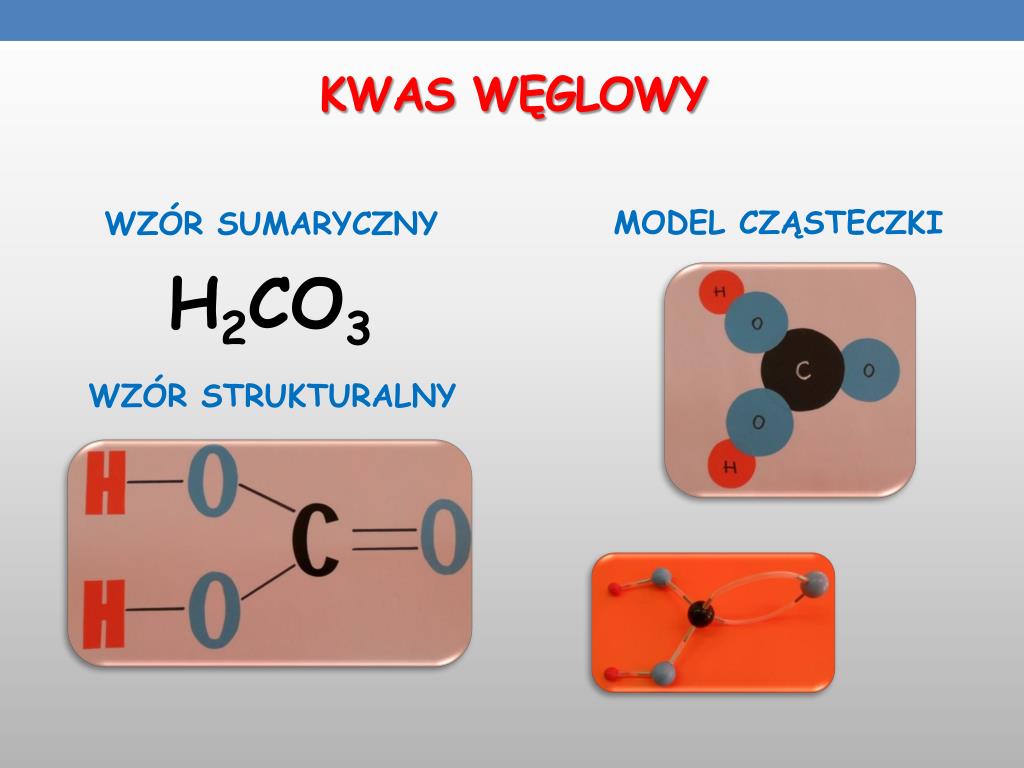
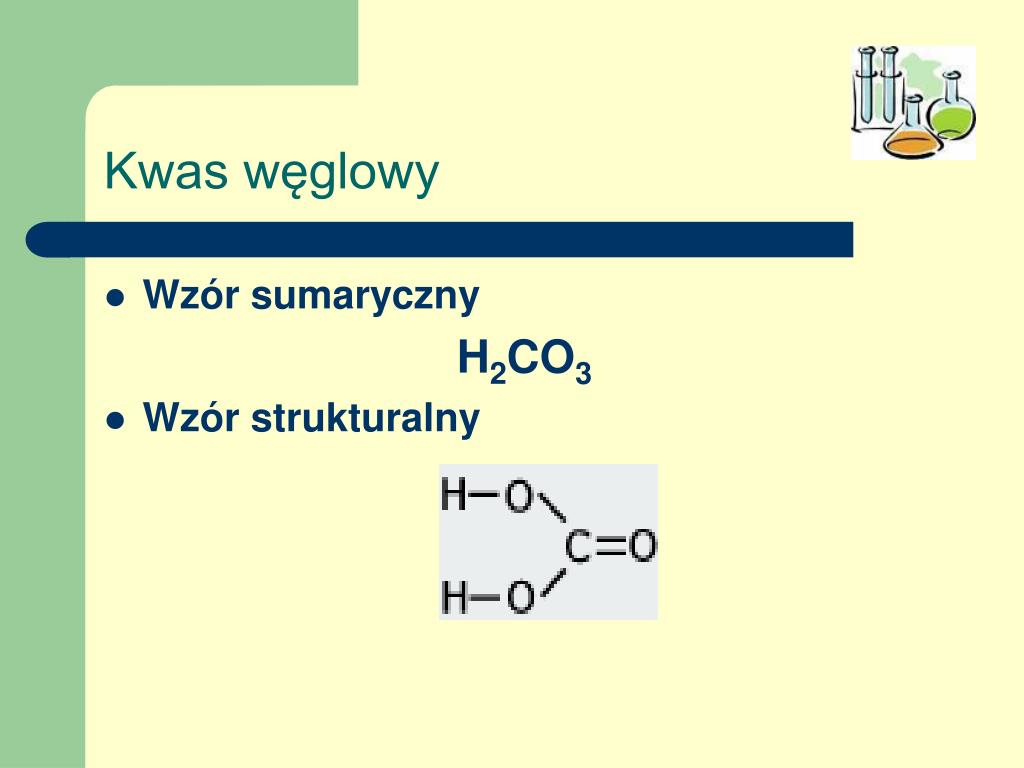
Wzór sumaryczny kwasu węglowego to H2CO3. Wskazuje on, że w cząsteczce znajdują się dwa atomy wodoru, jeden atom węgla i trzy atomy tlenu. Jego masa molowa wynosi około 62,03 g/mol.
Struktura kwasu węglowego
Struktura kwasu węglowego składa się z atomu węgla centralnego. Jest on związany podwójnym wiązaniem z jednym atomem tlenu (C=O). Pozostałe dwa atomy tlenu są związane pojedynczymi wiązaniami z atomem węgla (C-O). Do każdego z tych atomów tlenu przyłączony jest atom wodoru (O-H).
Można to sobie wyobrazić jako grupę karbonylową (C=O) przyłączoną do dwóch grup hydroksylowych (-OH). Takie ułożenie atomów determinuje właściwości kwasu węglowego. Wpływa również na jego zdolność do dysocjacji i reakcji z innymi substancjami.
Ważnym aspektem struktury jest jej planarność. Atomy tworzące centralną część cząsteczki (H-O-C-O-H) leżą w jednej płaszczyźnie. Wynika to z obecności wiązania podwójnego między węglem a tlenem. Ogranicza to rotację wokół tego wiązania.
Dysocjacja kwasu węglowego
Kwas węglowy dysocjuje dwustopniowo w roztworach wodnych. W pierwszym etapie oddaje jeden proton (H+), tworząc jon wodorowęglanowy (HCO3-). Jest to słaby kwas, więc reakcja ta zachodzi w niewielkim stopniu.
H2CO3 ⇌ H+ + HCO3-
Jon wodorowęglanowy również może dysocjować. W drugim etapie oddaje kolejny proton, tworząc jon węglanowy (CO32-). Ta dysocjacja zachodzi jeszcze trudniej niż pierwsza, co oznacza, że jon węglanowy występuje w niewielkich stężeniach.
HCO3- ⇌ H+ + CO32-
Te procesy dysocjacji mają kluczowe znaczenie dla utrzymania stałego pH krwi. Biorą także udział w procesach buforowych w organizmach żywych.
Znaczenie kwasu węglowego w przyrodzie i przemyśle
Kwas węglowy i jego sole (węglany i wodorowęglany) odgrywają istotną rolę w regulacji pH w różnych systemach. W naturalnych wodach, takich jak oceany i jeziora, system węglanowy pomaga w utrzymaniu stabilnego pH, co jest niezbędne dla życia organizmów wodnych. Ma także duży wpływ na procesy atmosferyczne, związane z efektem cieplarnianym.
W przemyśle spożywczym, dwutlenek węgla, który jest prekursorem kwasu węglowego, jest wykorzystywany do produkcji napojów gazowanych. Nadaje im charakterystyczny smak i orzeźwienie. Używa się go także jako składnik mieszanin chłodzących.
W medycynie, system buforowy oparty na kwasie węglowym i wodorowęglanach jest niezwykle ważny dla utrzymania stałego pH krwi. Zaburzenia tego systemu mogą prowadzić do poważnych problemów zdrowotnych, takich jak kwasica lub zasadowica.
Wpływ kwasu węglowego na środowisko
Kwas węglowy ma istotny wpływ na procesy geologiczne. Reaguje z minerałami, powodując ich wietrzenie i rozpuszczanie. Ten proces przyczynia się do powstawania jaskiń i innych formacji krasowych. To oddziałuje na jakość gleby i zasoby wód gruntowych.
Zwiększone stężenie dwutlenku węgla w atmosferze, prowadzące do zwiększonej zawartości kwasu węglowego w oceanach, powoduje zakwaszenie wód oceanicznych. To z kolei zagraża życiu organizmów morskich, szczególnie tych, które budują swoje szkielety i skorupy z węglanu wapnia, np. koralowce i skorupiaki.
Zrozumienie struktury i właściwości kwasu węglowego jest kluczowe dla zrozumienia wielu procesów zachodzących w przyrodzie. Pozwala to na podejmowanie świadomych działań na rzecz ochrony środowiska i zrównoważonego rozwoju. Redukcja emisji CO2 do atmosfery jest jednym z najważniejszych wyzwań stojących przed ludzkością.