Hej! Gotowi na podróż w świat chemii? Zajmiemy się dzisiaj dwoma ważnymi grupami związków: tlenkami i wodorotlenkami. Rozłóżmy to na czynniki pierwsze!
Czym są Tlenki?
Zacznijmy od tlenków. Tlenek to związek chemiczny, który zawiera tlen połączony z innym pierwiastkiem. Brzmi skomplikowanie? Spokojnie, zaraz to uprościmy. Pomyśl o rdzy na metalu – to właśnie tlenek!
Definicja jest prosta: tlenek = tlen + inny pierwiastek. Ważne jest, aby ten inny pierwiastek był mniej elektroujemny niż tlen. To oznacza, że tlen "zabiera" elektrony od tego drugiego pierwiastka. Dzięki temu tworzy się stabilne połączenie. Tlen jest bardzo reaktywny i chętnie łączy się z innymi pierwiastkami.
Przykłady Tlenków
Oto kilka przykładów tlenków, które spotykamy na co dzień:
- Tlenek żelaza (III) (Fe2O3) – to właśnie rdza! Powstaje, gdy żelazo reaguje z tlenem w obecności wilgoci.
- Tlenek węgla (IV) (CO2) – wydychamy go podczas oddychania. Jest też produktem spalania paliw.
- Tlenek krzemu (IV) (SiO2) – to główny składnik piasku i kwarcu.
- Tlenek wapnia (CaO) – to wapno palone, używane w budownictwie i rolnictwie.
Nazewnictwo Tlenków
Jak nazywać tlenki? To proste! Najpierw piszemy "tlenek", a potem nazwę pierwiastka, z którym tlen się połączył. Jeśli pierwiastek ma więcej niż jedną wartościowość, musimy to zaznaczyć w nazwie. Robimy to za pomocą cyfr rzymskich w nawiasie. Na przykład, tlenek żelaza (II) to FeO, a tlenek żelaza (III) to Fe2O3.
Czyli: tlenek + nazwa pierwiastka (+ wartościowość pierwiastka). Pamiętaj o wartościowości! To bardzo ważne, żeby poprawnie zidentyfikować dany tlenek. Wartościowość mówi nam, ile elektronów dany pierwiastek oddaje lub przyjmuje podczas tworzenia wiązania chemicznego.
Czym są Wodorotlenki?
Teraz przejdźmy do wodorotlenków. Wodorotlenek to związek chemiczny, który zawiera grupę hydroksylową (-OH) połączoną z metalem. Grupa hydroksylowa nadaje wodorotlenkom charakterystyczne właściwości. Wodorotlenki są często używane w przemyśle i w gospodarstwach domowych.
Definicja: wodorotlenek = metal + grupa hydroksylowa (-OH). Ważne jest, że łączy się ona z metalem. Grupa -OH składa się z atomu tlenu i atomu wodoru. To właśnie ona odpowiada za zasadowy charakter wodorotlenków.
Przykłady Wodorotlenków
Oto kilka przykładów wodorotlenków, które możesz znać:
- Wodorotlenek sodu (NaOH) – znany jako soda kaustyczna lub ług. Używany do produkcji mydła i papieru, a także do udrożniania rur.
- Wodorotlenek potasu (KOH) – podobny do wodorotlenku sodu, również używany w produkcji mydła i elektrolitów.
- Wodorotlenek wapnia (Ca(OH)2) – znany jako wapno gaszone. Używany w budownictwie i rolnictwie do odkwaszania gleby.
- Wodorotlenek magnezu (Mg(OH)2) – składnik mleczka magnezjowego, używanego jako lek na zgagę i problemy trawienne.
Nazewnictwo Wodorotlenków
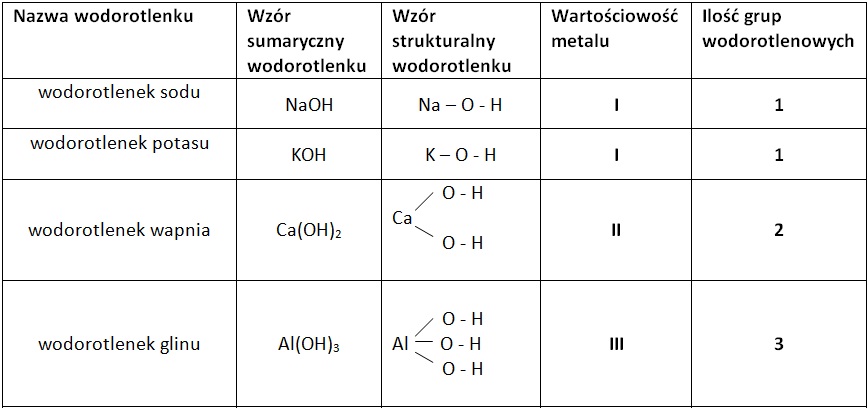
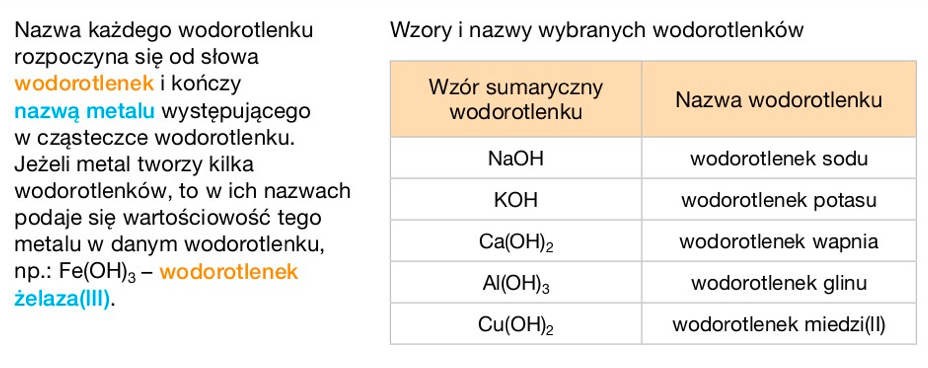
Nazewnictwo wodorotlenków jest bardzo proste. Zaczynamy od słowa "wodorotlenek", a następnie dodajemy nazwę metalu, z którym grupa hydroksylowa jest połączona. Jeśli metal ma więcej niż jedną wartościowość, tak jak w przypadku tlenków, zaznaczamy to cyfrą rzymską w nawiasie. Na przykład, wodorotlenek żelaza (II) to Fe(OH)2, a wodorotlenek żelaza (III) to Fe(OH)3.
Zatem: wodorotlenek + nazwa metalu (+ wartościowość metalu). Podobnie jak w przypadku tlenków, wartościowość jest kluczowa! Określa ona, ile grup hydroksylowych jest połączonych z danym atomem metalu. To wpływa na właściwości i reaktywność wodorotlenku.
Różnice między Tlenkami a Wodorotlenkami
Podsumujmy główne różnice między tlenkami i wodorotlenkami. Tlenki to związki tlenu z innymi pierwiastkami (zazwyczaj niemetalami lub metalami). Wodorotlenki to związki metali z grupą hydroksylową (-OH).
Tlenki mogą mieć charakter kwasowy, zasadowy lub obojętny. Na przykład, tlenki niemetali (np. CO2) zazwyczaj tworzą kwasy po rozpuszczeniu w wodzie, a tlenki metali (np. Na2O) tworzą zasady. Wodorotlenki natomiast mają charakter zasadowy. Reagują z kwasami, tworząc sole i wodę.
Inaczej mówiąc, tlenki to bardziej ogólna grupa związków. Wodorotlenki to podgrupa związków, które charakteryzują się obecnością grupy hydroksylowej i zasadowym charakterem. Pamiętaj o tych różnicach, żeby dobrze je rozróżniać.
Jak Przygotować się do Sprawdzianu?
Skoro już wiesz, czym są tlenki i wodorotlenki, jak przygotować się do sprawdzianu? Po pierwsze, powtórz definicje i przykłady. Po drugie, naucz się poprawnie nazywać te związki. Po trzecie, spróbuj rozwiązać kilka zadań z nazewnictwa i wzorów. Po czwarte, zrozum różnice między tlenkami a wodorotlenkami.
Spróbuj również znaleźć więcej przykładów tlenków i wodorotlenków w swoim otoczeniu. Im więcej będziesz widział zastosowań tych związków w życiu codziennym, tym łatwiej będzie Ci je zapamiętać i zrozumieć. Pamiętaj, chemia jest wszędzie!
I pamiętaj, nie stresuj się! Zrozumienie podstaw to klucz do sukcesu. Powodzenia na sprawdzianie!