Chemia organiczna potrafi być wyzwaniem, ale nie martw się! Razem przejdziemy przez alkany, alkeny i alkiny. Rozłożymy te pojęcia na czynniki pierwsze, abyś mógł bez problemu napisać sprawdzian "Nowej Ery".
Węglowodory: Podstawa wszystkiego
Na początek, musimy zrozumieć, czym są węglowodory. Są to związki organiczne składające się wyłącznie z atomów węgla (C) i wodoru (H). To one stanowią fundament większości paliw i wielu innych substancji, które nas otaczają. Pomyśl o benzynie, gazie ziemnym czy plastiku – to wszystko węglowodory!
Właściwości węglowodorów zależą od tego, jak atomy węgla są połączone ze sobą. Mogą tworzyć łańcuchy proste, rozgałęzione, a nawet pierścienie. Rodzaj wiązań między atomami węgla również ma ogromne znaczenie. Właśnie tutaj wkraczają alkany, alkeny i alkiny.
Alkany: Nasycone związki węgla
Alkany to węglowodory nasycone. Oznacza to, że między atomami węgla występują tylko i wyłącznie wiązania pojedyncze. Mają ogólny wzór CnH2n+2, gdzie "n" oznacza liczbę atomów węgla w cząsteczce. Są to związki stosunkowo mało reaktywne.
Przykłady alkanów:
- Metan (CH4): Główny składnik gazu ziemnego, używany do ogrzewania domów.
- Etan (C2H6): Wykorzystywany jako paliwo i w przemyśle chemicznym.
- Propan (C3H8): Znajdziesz go w butlach gazowych używanych do kuchenek turystycznych.
- Butan (C4H10): Używany w zapalniczkach.
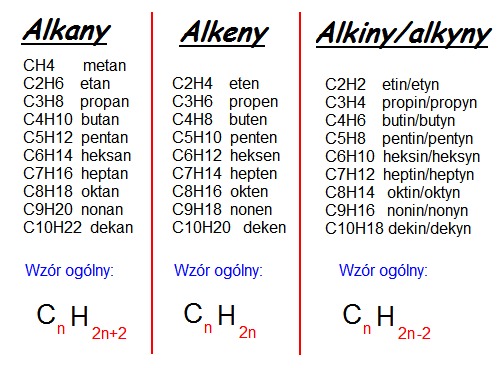
Nazewnictwo alkanów jest proste. Dodajesz przedrostek oznaczający liczbę atomów węgla (np. "met-" dla 1, "et-" dla 2, "prop-" dla 3, "but-" dla 4, "pent-" dla 5, "heks-" dla 6, itd.) i końcówkę "-an". Zatem alkan zawierający 5 atomów węgla to pentan.
Alkeny: Wiązania podwójne w akcji
Alkeny to węglowodory nienasycone, które zawierają przynajmniej jedno wiązanie podwójne między atomami węgla. Ich ogólny wzór to CnH2n. Obecność wiązania podwójnego sprawia, że są bardziej reaktywne niż alkany.
Przykłady alkenów:
- Eten (C2H4) (znany również jako etylen): Używany do produkcji tworzyw sztucznych, takich jak polietylen (PE). Przyspiesza dojrzewanie owoców.
- Propen (C3H6): Wykorzystywany do produkcji polipropylenu (PP), innego popularnego tworzywa sztucznego.
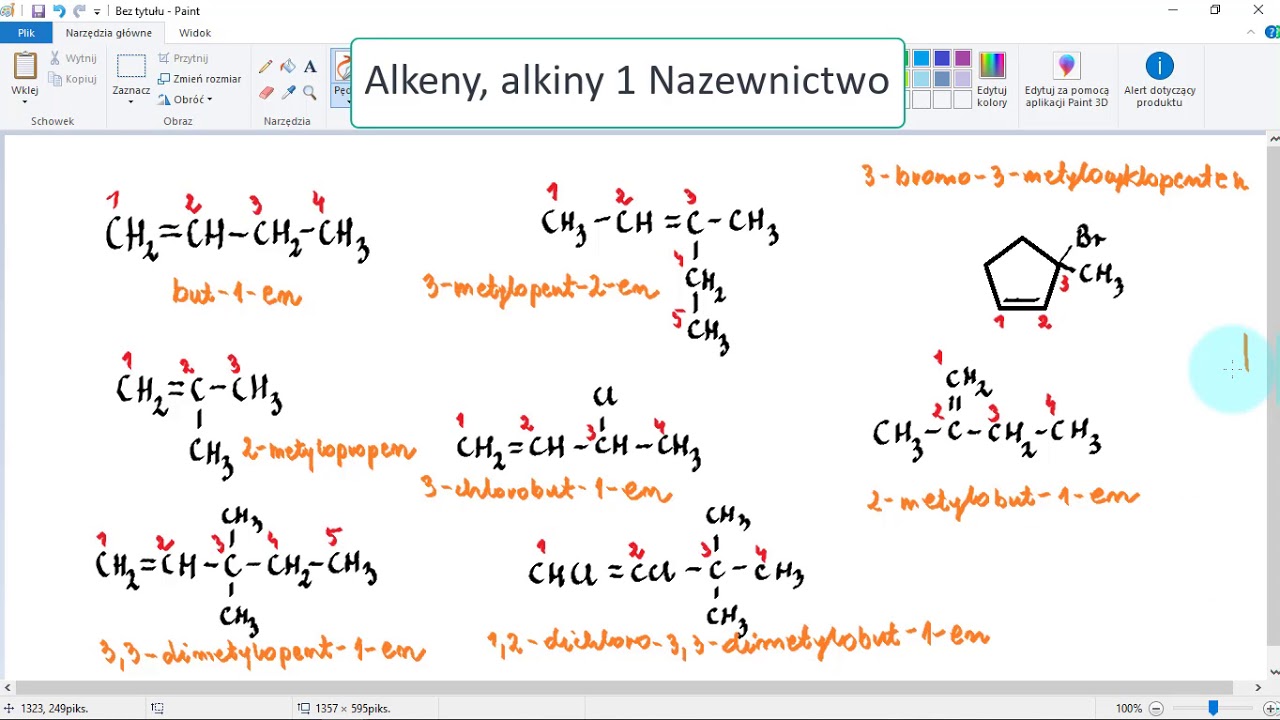
Nazewnictwo alkenów jest podobne do alkanów, ale zamiast końcówki "-an" używamy "-en". Musimy również wskazać, przy którym atomie węgla zaczyna się wiązanie podwójne, np. but-1-en oznacza, że wiązanie podwójne znajduje się między pierwszym a drugim atomem węgla w łańcuchu.
Alkiny: Potrójna moc wiązania
Alkiny to również węglowodory nienasycone, ale tym razem zawierają przynajmniej jedno wiązanie potrójne między atomami węgla. Mają ogólny wzór CnH2n-2. Wiązanie potrójne czyni je jeszcze bardziej reaktywnymi niż alkeny.
Przykładem alkinu jest:
- Etyn (C2H2) (znany również jako acetylen): Używany w palnikach acetylenowo-tlenowych do spawania i cięcia metali.
Nazewnictwo alkinów jest analogiczne do alkenów, ale używamy końcówki "-in". Podobnie jak w alkenach, musimy wskazać położenie wiązania potrójnego, np. but-1-yn.
Reakcje charakterystyczne
Alkany, alkeny i alkiny podlegają różnym reakcjom chemicznym. Rozważymy te najważniejsze.
Reakcje alkanów:
- Spalanie: Alkany spalają się w obecności tlenu, tworząc dwutlenek węgla i wodę. To właśnie wykorzystujemy, spalając gaz ziemny w kuchence.
- Substytucja (podstawianie): Atom wodoru w alkanie może zostać zastąpiony innym atomem, np. chlorem w reakcji chlorowania.
Reakcje alkenów i alkinów:
- Addycja (przyłączanie): Wiązanie podwójne lub potrójne "rozrywa się", a do atomów węgla przyłączają się inne atomy lub grupy atomów. Przykładem jest addycja wodoru (uwodornianie), w wyniku której alken przekształca się w alkan, a alkin w alken lub alkan.
- Polimeryzacja: Wiele cząsteczek alkenu (monomerów) łączy się ze sobą, tworząc długi łańcuch polimeru, np. etylen polimeryzuje do polietylenu.
- Spalanie: Podobnie jak alkany, alkeny i alkiny ulegają spalaniu.
Podsumowanie: Kluczowe różnice
Aby łatwiej zapamiętać różnice między alkanami, alkenami i alkinami, spójrz na to zestawienie:
- Alkany: Wiązania pojedyncze (nasycone), wzór CnH2n+2, stosunkowo mało reaktywne.
- Alkeny: Jedno wiązanie podwójne, wzór CnH2n, bardziej reaktywne.
- Alkiny: Jedno wiązanie potrójne, wzór CnH2n-2, bardzo reaktywne.
Pamiętaj, że zrozumienie struktury i reaktywności tych związków jest kluczowe do sukcesu na sprawdzianie "Nowej Ery". Powodzenia!