Otrzymywanie wodorotlenków to fundamentalne zagadnienie w chemii nieorganicznej. Warto poświęcić mu dużo uwagi. Zapewni to uczniom solidne podstawy.
Sposoby Otrzymywania Wodorotlenków
Istnieje kilka głównych metod otrzymywania wodorotlenków. Każda z nich opiera się na innych właściwościach pierwiastków. Wiedza o tych metodach pozwala przewidywać właściwości chemiczne substancji.
Reakcja Metali Aktywnych z Wodą
Metale grupy pierwszej (litowce) i drugiej (berylowce, z wyjątkiem berylu) reagują gwałtownie z wodą. W wyniku tej reakcji powstaje wodorotlenek metalu i wodór. Reakcję tę najlepiej demonstrować z litowcami, ze względu na ich wysoką reaktywność, chociaż trzeba zachować ostrożność. Uczniowie często mylą aktywność metali z ich masą atomową. Należy im wytłumaczyć, że to potencjał standardowy decyduje o reaktywności.
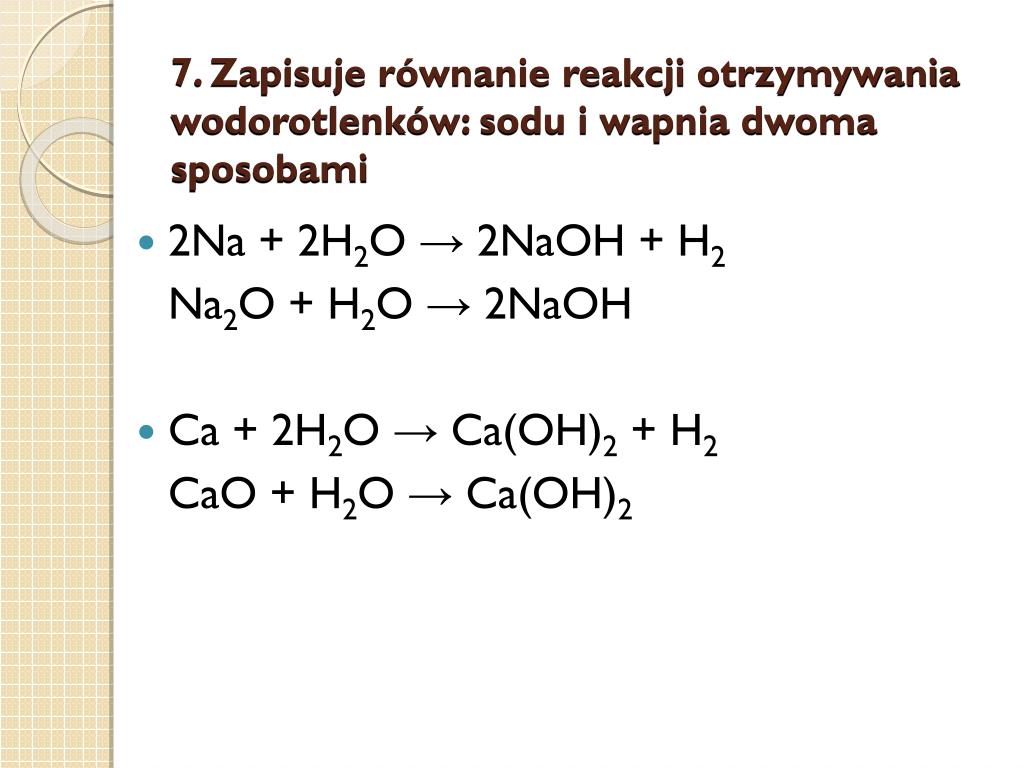
Przykład: 2Na + 2H2O → 2NaOH + H2. Ważne jest, aby pokazać to doświadczalnie. Uczniowie zapamiętują to dużo lepiej. Należy też omówić względy bezpieczeństwa podczas wykonywania tego doświadczenia.
Reakcja Tlenków Metali z Wodą
Tlenki metali aktywnych reagują z wodą, tworząc wodorotlenki. Tlenki te mają charakter zasadowy. Rozpuszczanie ich w wodzie prowadzi do powstania roztworu zasadowego. Często mylone są z tlenkami amfoterycznymi, które mogą reagować zarówno z kwasami, jak i zasadami. Warto to wyraźnie rozróżnić.
Przykład: CaO + H2O → Ca(OH)2. Dobrym przykładem jest wapno gaszone, czyli wodorotlenek wapnia. Można pokazać ten proces w formie prostego doświadczenia.
Reakcja Soli z Zasadami
Reakcja soli z zasadami prowadzi do powstania wodorotlenku, jeśli wodorotlenek ten jest nierozpuszczalny w wodzie (strąca się osad). Jest to reakcja wymiany. Warunkiem zajścia tej reakcji jest powstanie osadu. Uczniowie często zapominają o warunku nierozpuszczalności produktu.
Przykład: CuCl2 + 2NaOH → Cu(OH)2↓ + 2NaCl. Osad wodorotlenku miedzi(II) jest niebieski. Można wykorzystać tę reakcję jako efektowną demonstrację.
Elektroliza Roztworów Soli
Podczas elektrolizy roztworów niektórych soli można otrzymać wodorotlenki. Proces ten zachodzi na katodzie. Powstaje tam wodór i jony wodorotlenkowe. Metoda ta jest bardziej złożona. Zazwyczaj omawia się ją na wyższym poziomie nauczania. Często uczniowie mylą proces elektrolizy z prostym rozpuszczaniem soli w wodzie.
Przykład: Elektroliza roztworu NaCl prowadzi do powstania NaOH, Cl2 i H2. Ważne jest zrozumienie, że zachodzą tu reakcje redoks.
Wskazówki dla Nauczycieli
Wyjaśniając reakcje otrzymywania wodorotlenków, warto skupić się na praktycznych przykładach. Można pokazać doświadczenia. Pozwolą one na lepsze zrozumienie materiału. Należy wyjaśnić, dlaczego dana reakcja zachodzi.
- Demonstracje: Przeprowadzaj proste i bezpieczne demonstracje. Pozwolą one na wizualizację procesu. Reakcja metalu z wodą czy tlenku z wodą to doskonałe przykłady.
- Modele: Używaj modeli atomów i cząsteczek. Pomoże to uczniom zrozumieć, jak atomy łączą się, tworząc wodorotlenki.
- Zadania: Dawaj zadania obliczeniowe i problemowe. Zmuszą one uczniów do myślenia i zastosowania wiedzy w praktyce.
Typowe Błędy i Nieporozumienia
Uczniowie często popełniają błędy podczas pisania wzorów sumarycznych wodorotlenków. Zapominają o wartościowości metalu. Powoduje to błędne zapisy wzorów. Innym problemem jest mylenie wodorotlenków z tlenkami.
- Wartościowość: Upewnij się, że uczniowie dobrze rozumieją pojęcie wartościowości. Wyjaśnij, jak wpływa ona na wzór wodorotlenku.
- Rozpuszczalność: Omów rozpuszczalność wodorotlenków w wodzie. Wykorzystaj tablice rozpuszczalności.
- Nazewnictwo: Ćwicz nazewnictwo wodorotlenków. Wyjaśnij, jak tworzyć poprawne nazwy systematyczne.
Sposoby na Uatrakcyjnienie Tematu
Otrzymywanie wodorotlenków może być ciekawe. Wystarczy użyć odpowiednich metod. Można wykorzystać gry edukacyjne. Pozwolą one na naukę poprzez zabawę. Można też zorganizować konkursy wiedzy.
- Gry: Wykorzystaj gry planszowe lub online. Utrwalą one wiedzę o reakcjach otrzymywania wodorotlenków.
- Projekty: Zadaj uczniom projekty badawcze. Niech zbadają właściwości różnych wodorotlenków.
- Kontekst: Pokaż, gdzie w życiu codziennym można spotkać wodorotlenki. Zastosowanie w przemyśle, medycynie czy kosmetyce.
Podsumowując, nauczanie o reakcjach otrzymywania wodorotlenków wymaga cierpliwości i kreatywności. Stosowanie różnych metod dydaktycznych. Powinno to pomóc uczniom w zrozumieniu i zapamiętaniu tego ważnego zagadnienia.