Cześć! Dzisiaj zajmiemy się czymś, co nazywa się obliczenia wagowe. To zagadnienie, które może wydawać się skomplikowane na początku, ale obiecuję, że krok po kroku wszystko stanie się jasne. Spróbujemy zrozumieć to na przykładach, które znasz z życia codziennego.
Co to są obliczenia wagowe?
Obliczenia wagowe to nic innego jak obliczenia związane z wagą różnych substancji, które są potrzebne do przygotowania mieszanek lub roztworów o określonym stężeniu. Myśl o tym jak o gotowaniu! Często musisz odmierzyć odpowiednią ilość składników, żeby potrawa wyszła idealna. W chemii i fizyce jest podobnie.
Wyobraź sobie, że chcesz zrobić lemoniadę. Potrzebujesz wody, soku z cytryny i cukru. Obliczenia wagowe pomagają Ci ustalić, ile cukru i soku z cytryny musisz dodać do określonej ilości wody, żeby lemoniada miała idealny smak. Zamiast smaku, w chemii mówimy o stężeniu.
Kluczowe pojęcia, które musisz znać to: masa (waga), stężenie procentowe, rozpuszczalnik i substancja rozpuszczana. Omówimy je po kolei.
Masa (Waga)
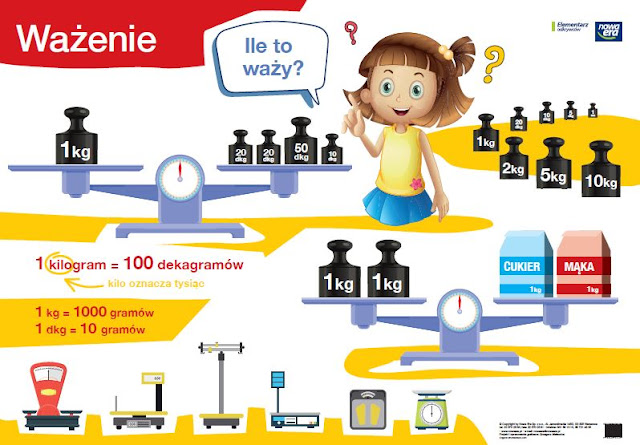
Masa to ilość materii zawartej w danym obiekcie. Często używamy słów "masa" i "waga" zamiennie, choć technicznie rzecz biorąc, waga to siła, z jaką Ziemia przyciąga dany obiekt. W obliczeniach wagowych zazwyczaj używamy masy wyrażonej w gramach (g) lub kilogramach (kg). Pamiętaj, że 1 kg = 1000 g.
Na przykład, jeśli masz paczkę mąki, która waży 1 kg, to znaczy, że jej masa wynosi 1 kg. To proste, prawda? Masa jest podstawą do dalszych obliczeń.
Stężenie Procentowe
Stężenie procentowe (oznaczane jako %) to sposób wyrażenia, ile substancji rozpuszczonej znajduje się w roztworze. Mówi nam, jaki procent masy całego roztworu stanowi masa substancji rozpuszczonej. Wzór na stężenie procentowe to: Stężenie procentowe = (masa substancji rozpuszczonej / masa roztworu) * 100%
Wyobraź sobie, że masz 100g roztworu soli, w którym znajduje się 10g soli. Stężenie procentowe tego roztworu wynosi (10g / 100g) * 100% = 10%. Oznacza to, że w 100 gramach tego roztworu znajduje się 10 gramów soli.
Inny przykład: roztwór glukozy o stężeniu 5% oznacza, że w 100 gramach roztworu znajduje się 5 gramów glukozy. Reszta to rozpuszczalnik, najczęściej woda.
Rozpuszczalnik i Substancja Rozpuszczana
Rozpuszczalnik to substancja, w której rozpuszcza się inna substancja. Najczęściej rozpuszczalnikiem jest woda. Na przykład, w przypadku lemoniady, wodą jest rozpuszczalnik.
Substancja rozpuszczana to substancja, która rozpuszcza się w rozpuszczalniku. W przypadku lemoniady, substancjami rozpuszczonymi są sok z cytryny i cukier.
Roztwór to mieszanina rozpuszczalnika i substancji rozpuszczonej. Czyli lemoniada to roztwór wody, soku z cytryny i cukru.
Przykłady Obliczeń Wagowych
Teraz, kiedy już znamy podstawowe pojęcia, przejdźmy do kilku przykładów obliczeń wagowych.
Przykład 1: Przygotowanie roztworu o określonym stężeniu procentowym
Chcesz przygotować 200g roztworu soli o stężeniu 15%. Ile soli i wody potrzebujesz?
Krok 1: Oblicz masę soli. Stężenie procentowe = (masa soli / masa roztworu) * 100% 15% = (masa soli / 200g) * 100% Masa soli = (15% * 200g) / 100% = 30g
Krok 2: Oblicz masę wody. Masa roztworu = masa soli + masa wody 200g = 30g + masa wody Masa wody = 200g - 30g = 170g
Odpowiedź: Potrzebujesz 30g soli i 170g wody, żeby przygotować 200g roztworu soli o stężeniu 15%.
Przykład 2: Obliczenie stężenia procentowego roztworu
Rozpuściłeś 25g cukru w 125g wody. Jakie jest stężenie procentowe tego roztworu?
Krok 1: Oblicz masę roztworu. Masa roztworu = masa cukru + masa wody Masa roztworu = 25g + 125g = 150g
Krok 2: Oblicz stężenie procentowe. Stężenie procentowe = (masa cukru / masa roztworu) * 100% Stężenie procentowe = (25g / 150g) * 100% = 16.67% (w przybliżeniu)
Odpowiedź: Stężenie procentowe tego roztworu cukru wynosi około 16.67%.
Przykład 3: Obliczenie masy roztworu
Chcesz użyć 5g substancji chemicznej, a masz do dyspozycji roztwór o stężeniu 10%. Jaką masę tego roztworu musisz odmierzyć?
Krok 1: Ustal zależność. 10% roztwór oznacza, że w 100g roztworu znajduje się 10g substancji.
Krok 2: Oblicz masę roztworu potrzebną do uzyskania 5g substancji. Możemy użyć proporcji: 10g substancji --- 100g roztworu 5g substancji --- x g roztworu x = (5g * 100g) / 10g = 50g
Odpowiedź: Musisz odmierzyć 50g roztworu o stężeniu 10%, żeby uzyskać 5g substancji.
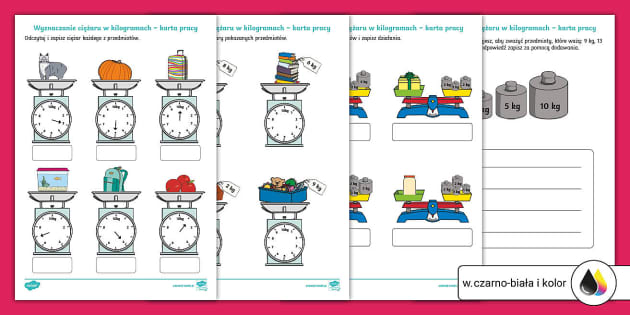
Karty Pracy z Obliczeń Wagowych (Klasa 3)
Karty pracy z obliczeń wagowych dla klasy 3 to zbiór zadań i ćwiczeń, które pomagają uczniom w praktycznym zastosowaniu wiedzy o stężeniach procentowych, masie rozpuszczalnika i substancji rozpuszczonej. Zadania te często obejmują przygotowywanie roztworów o określonym stężeniu, obliczanie stężenia procentowego na podstawie danych, czy też określanie masy substancji potrzebnej do przygotowania roztworu.
Pracując z kartami pracy, możesz spotkać się z różnymi typami zadań, takimi jak: obliczanie ilości cukru potrzebnej do przygotowania określonej ilości syropu o danym stężeniu, obliczanie stężenia procentowego roztworu soli kuchennej, czy też obliczanie ilości wody potrzebnej do rozcieńczenia roztworu kwasu.
Pamiętaj, żeby zawsze dokładnie czytać treść zadania, zrozumieć, co jest dane, a co trzeba obliczyć. Następnie, skorzystaj ze wzorów, które omówiliśmy wcześniej i podstaw odpowiednie wartości. Nie zapomnij o jednostkach! Zawsze zapisuj jednostki (g, kg, %), żeby uniknąć pomyłek.
Podsumowanie
Obliczenia wagowe to ważny element wielu dziedzin nauki i życia codziennego. Zrozumienie podstawowych pojęć, takich jak masa, stężenie procentowe, rozpuszczalnik i substancja rozpuszczona, oraz umiejętność rozwiązywania prostych zadań, to klucz do sukcesu. Pamiętaj o praktyce! Im więcej zadań rozwiążesz, tym lepiej zrozumiesz te zagadnienia. Powodzenia!