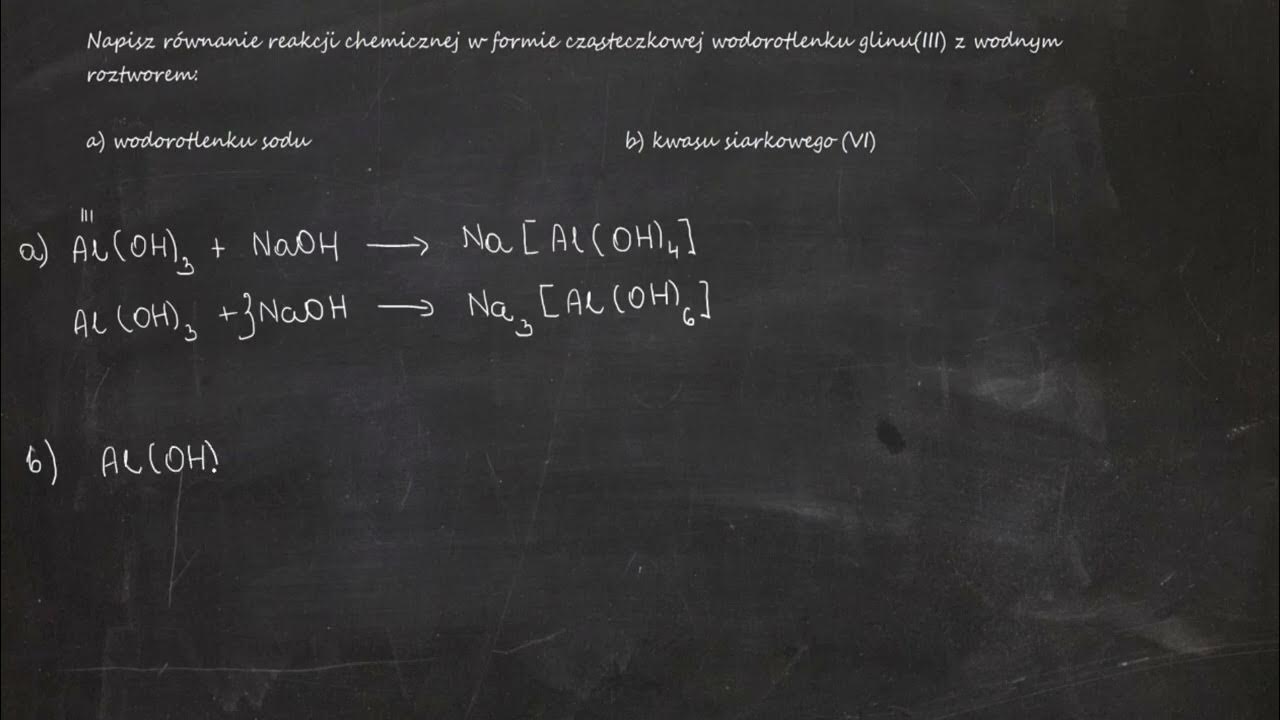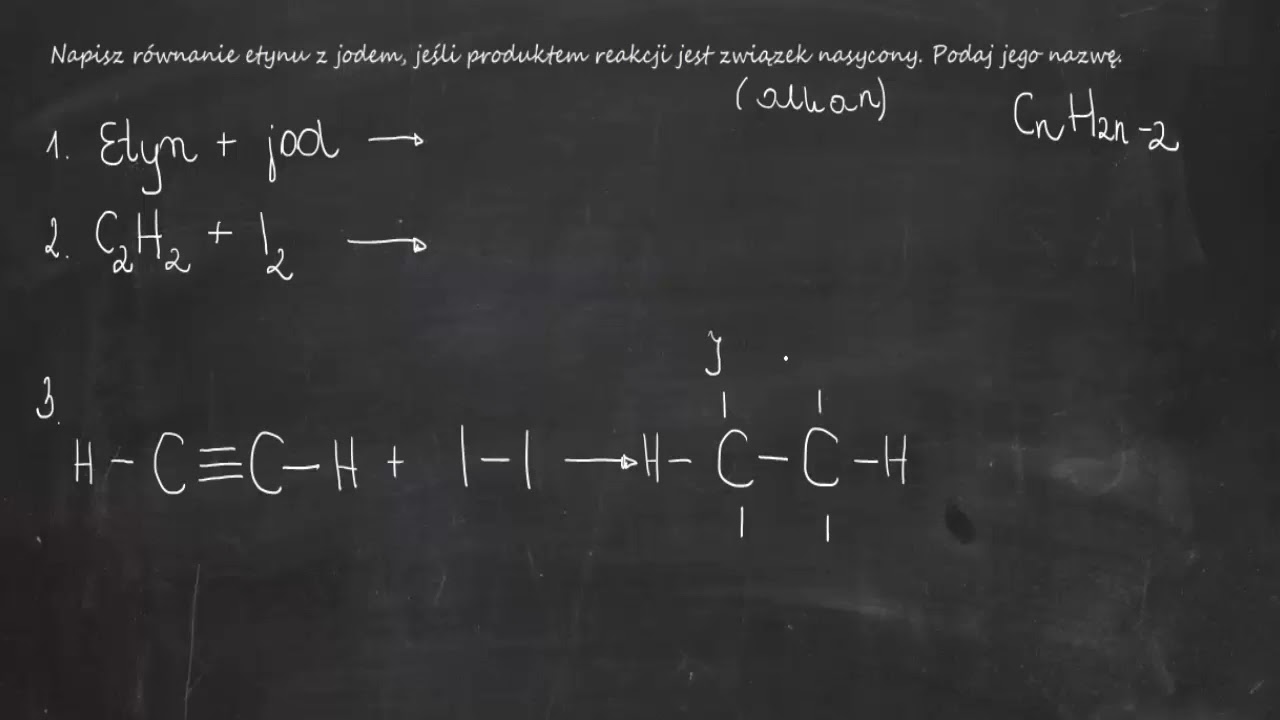Reakcja etynu z jodem jest fascynującym przykładem reakcji addycji elektrofilowej. Możemy ją wykorzystać do zilustrowania koncepcji wiązań wielokrotnych w chemii organicznej. Jest to też okazja do wprowadzenia pojęcia Markovnikov's rule, choć w pewnym stopniu uproszczonym.
Równanie Reakcji Etynu z Jodem
Zapiszmy to równanie chemiczne. Pamiętajmy o współczynnikach stechiometrycznych. Wyjaśnijmy, że etyn, czyli acetylen, ma wiązanie potrójne między atomami węgla.
C₂H₂ + I₂ → C₂H₂I₂
C₂H₂I₂ + I₂ → C₂H₂I₄
Uczniowie powinni rozumieć, że reakcja zachodzi dwuetapowo. Najpierw następuje addycja jednej cząsteczki jodu. Potem następuje addycja drugiej cząsteczki jodu. Ważne jest, aby podkreślić, że wiązanie potrójne przekształca się kolejno w wiązanie podwójne, a następnie w wiązanie pojedyncze.
Wyjaśnienie Krok po Kroku
Rozpocznijmy od struktury etynu (C₂H₂). Zwróćmy uwagę na obecność wiązania potrójnego. Zilustrujmy, jak wiązanie potrójne składa się z jednego wiązania sigma (σ) i dwóch wiązań pi (π). To właśnie wiązania pi są podatne na rozerwanie podczas reakcji addycji.
Następnie pokażmy cząsteczkę jodu (I₂). Jod jest pierwiastkiem z grupy fluorowców. Wyjaśnijmy, że cząsteczka jodu jest niepolarna, ale pod wpływem zbliżenia do gęstości elektronowej wiązania π w etynie może ulec polaryzacji. Powoduje to, że jeden atom jodu staje się bardziej elektrofilowy, czyli "lubiący elektrony".
W pierwszym etapie reakcji, elektrofilowy atom jodu atakuje wiązanie π w etynie. Wiązanie π pęka, a atom jodu tworzy wiązanie z jednym z atomów węgla. Drugi atom jodu przyłącza się do drugiego atomu węgla. Powstaje dijodoeten (C₂H₂I₂). Produktem pośrednim jest karbokation cykliczny z mostkiem jodoniowym. Jest to ważne dla zrozumienia stereochemii produktu.
W drugim etapie, proces powtarza się. Druga cząsteczka jodu atakuje wiązanie podwójne w dijodoetenie. Wiązanie podwójne pęka, a dwa atomy jodu przyłączają się do atomów węgla. Powstaje tetrajodoetan (C₂H₂I₄). Ważne jest, aby uczniowie zrozumieli, że reakcja addycji powoduje zmniejszenie liczby wiązań π.
Typowe Błędy i Jak Ich Unikać
Częstym błędem jest pomijanie drugiego etapu reakcji. Uczniowie często zapominają, że etyn może przyłączyć aż dwie cząsteczki jodu. Podkreślmy, że reakcja zachodzi dopóki istnieją wiązania π.
Innym błędem jest nieprawidłowe rysowanie struktur związków organicznych. Upewnijmy się, że uczniowie potrafią prawidłowo przedstawić wiązania potrójne, podwójne i pojedyncze. Można użyć modeli molekularnych, aby lepiej zwizualizować przestrzenny układ atomów.
Uczniowie mogą mieć trudności ze zrozumieniem pojęcia elektrofila. Wyjaśnijmy, że elektrofil to cząsteczka lub jon, który poszukuje elektronów. W reakcji etynu z jodem, jod pełni rolę elektrofila.
Pamiętajmy o używaniu poprawnej nomenklatury chemicznej. Konsekwentne stosowanie nazw systematycznych ułatwia uczniom zrozumienie i zapamiętanie nazw związków organicznych.
Jak Uatrakcyjnić Zajęcia?
Można użyć modeli molekularnych, aby uczniowie mogli "dotknąć" i zobaczyć, jak zmienia się struktura cząsteczki podczas reakcji. Modele ułatwiają zrozumienie przestrzennego układu atomów i wiązań.
Animacje komputerowe mogą pomóc w wizualizacji mechanizmu reakcji. Pokażmy, jak elektrony przemieszczają się podczas ataku elektrofilowego. To pozwala na lepsze zrozumienie dynamicznego charakteru reakcji.
Zorganizujmy quiz lub grę interaktywną. Sprawdźmy, czy uczniowie rozumieją, jak przebiega reakcja i jakie są produkty. Można też poprosić uczniów o samodzielne napisanie równań reakcji z innymi halogenami, np. z chlorem lub bromem.
Można zaproponować uczniom, aby sami poszukali informacji na temat zastosowań reakcji addycji w przemyśle chemicznym. Na przykład, reakcje addycji są wykorzystywane do produkcji polimerów i innych ważnych związków organicznych.
Wykorzystajmy analogie z życia codziennego. Można porównać reakcję addycji do "doklejania" czegoś do istniejącego obiektu. Na przykład, dodawanie przypraw do potrawy jest pewnego rodzaju "addycją".
Podkreślmy, że zrozumienie mechanizmów reakcji organicznych jest kluczowe dla dalszej nauki chemii. Reakcja etynu z jodem jest dobrym przykładem, który pozwala na wprowadzenie wielu ważnych pojęć i zasad.