Hej! Zastanawiałeś się kiedyś, dlaczego niektóre rzeczy łączą się ze sobą, a inne nie? Albo jak to się dzieje, że z prostych składników powstają zupełnie nowe substancje? Kluczem do zrozumienia tych zjawisk jest poznanie sposobu, w jaki łączą się ze sobą atomy i jak zapisujemy to w postaci równań reakcji chemicznych.
Czym są atomy i cząsteczki?
Wyobraź sobie, że wszystko wokół nas, od powietrza, którym oddychasz, po jedzenie, które jesz, zbudowane jest z maleńkich, niewidocznych gołym okiem cegiełek. Te cegiełki to właśnie atomy. Atom to najmniejsza część pierwiastka zachowująca jego właściwości. Atomy różnych pierwiastków różnią się od siebie budową, co wpływa na ich zdolność do łączenia się z innymi atomami.
Bardzo rzadko zdarza się, żeby atomy występowały samodzielnie w przyrodzie. Zazwyczaj łączą się ze sobą, tworząc większe struktury zwane cząsteczkami. Cząsteczka to zbiór co najmniej dwóch atomów połączonych ze sobą wiązaniem chemicznym. Na przykład, cząsteczka wody (H2O) składa się z dwóch atomów wodoru (H) i jednego atomu tlenu (O).
Jak łączą się atomy? Wiązania chemiczne
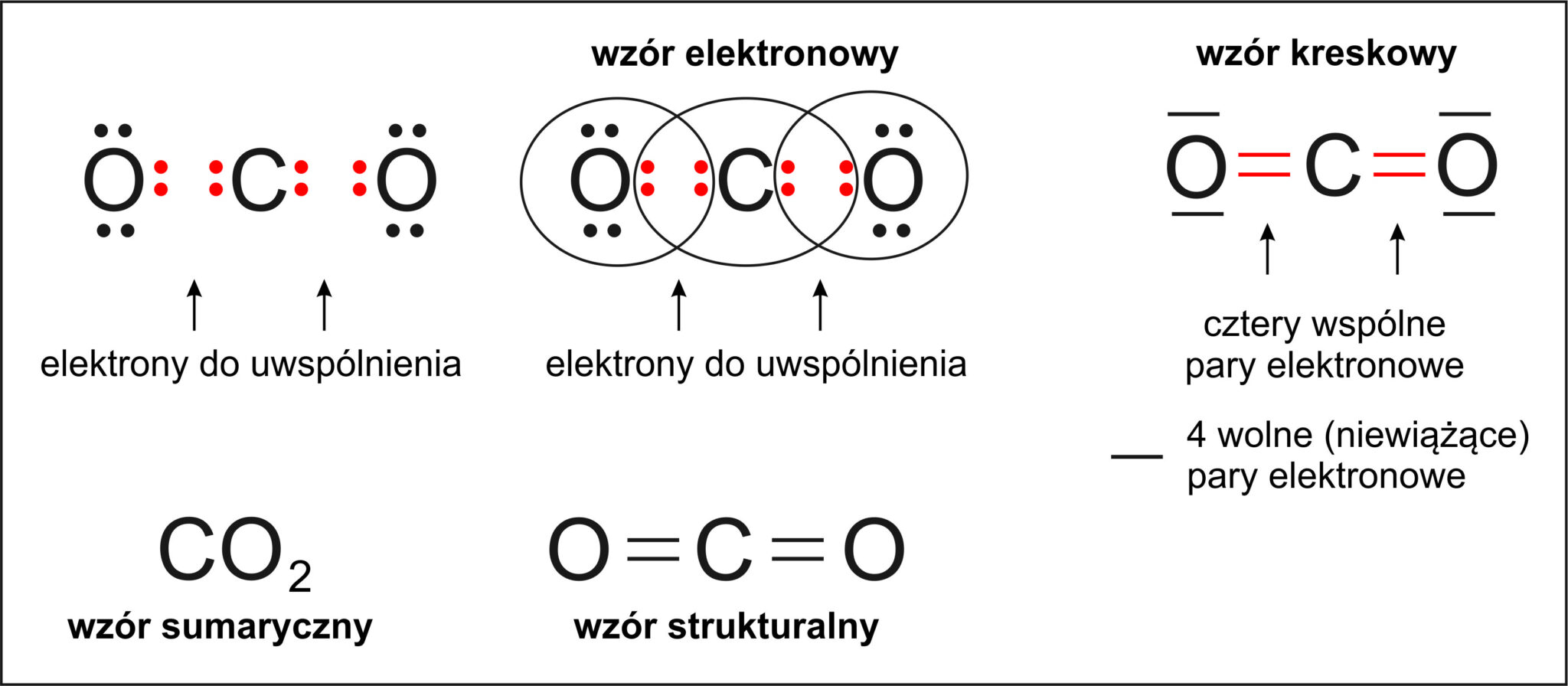
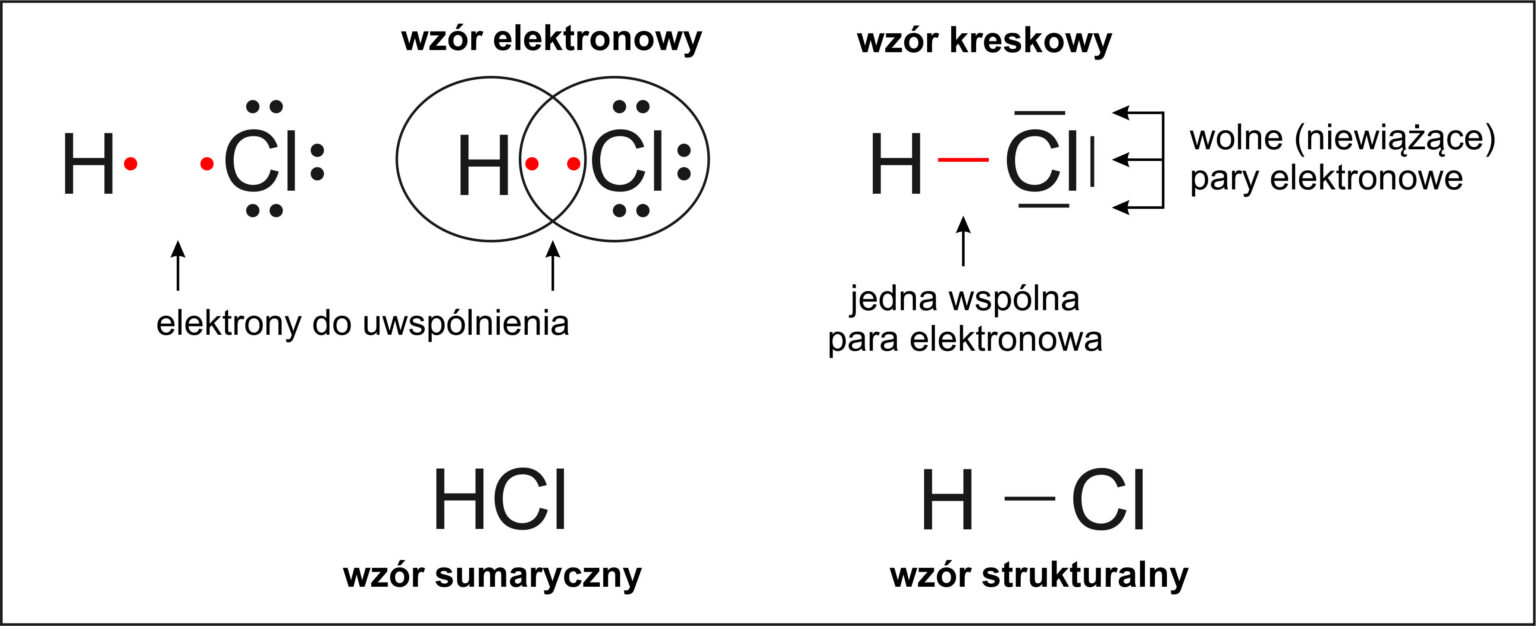
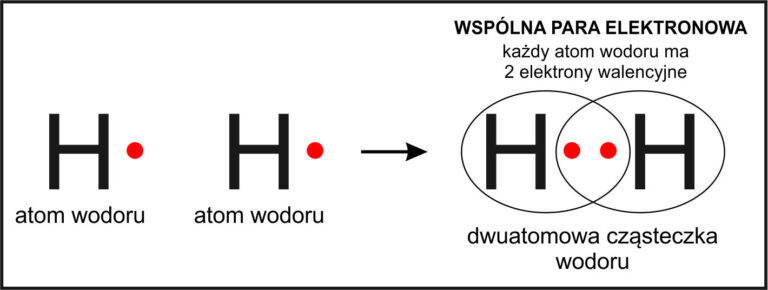
Atomy łączą się ze sobą, tworząc wiązania chemiczne. To tak, jakby miały magnesy, które przyciągają się do siebie. Istnieją różne rodzaje wiązań chemicznych, a to, jaki typ wiązania powstanie między dwoma atomami, zależy od ich właściwości. Dwa główne typy to wiązania kowalencyjne i wiązania jonowe. Rozważmy najpierw wiązanie kowalencyjne.
Wiązanie kowalencyjne powstaje wtedy, gdy atomy dzielą się swoimi elektronami. To tak, jakby dwoje przyjaciół dzieliło się zabawką. Dzięki temu oba atomy stają się bardziej stabilne. Przykładem jest cząsteczka metanu (CH4), gdzie jeden atom węgla dzieli się swoimi elektronami z czterema atomami wodoru.
Z kolei wiązanie jonowe powstaje wtedy, gdy jeden atom oddaje elektron innemu atomowi. To tak, jakby jeden przyjaciel dał zabawkę drugiemu. Atom, który oddaje elektron, staje się jonem dodatnim (kationem), a atom, który przyjmuje elektron, staje się jonem ujemnym (anionem). Jony o przeciwnych ładunkach przyciągają się do siebie, tworząc wiązanie jonowe. Przykładem jest chlorek sodu (NaCl), czyli sól kuchenna, gdzie atom sodu oddaje elektron atomowi chloru.
Reakcje chemiczne: Co się dzieje, gdy atomy zmieniają partnerów?
Reakcja chemiczna to proces, w którym atomy przegrupowują się, tworząc nowe cząsteczki. To tak, jakbyś miał klocki LEGO i rozkładał jeden model, żeby zbudować z nich coś zupełnie innego. Podczas reakcji chemicznych wiązania między atomami w jednych cząsteczkach ulegają zerwaniu, a następnie tworzą się nowe wiązania, tworząc inne cząsteczki. Substancje, które wchodzą w reakcję, nazywamy substratami, a substancje, które powstają w wyniku reakcji, nazywamy produktami.
Weźmy przykład spalania drewna. Drewno (głównie celuloza) reaguje z tlenem z powietrza. Podczas spalania wiązania między atomami węgla, wodoru i tlenu w celulozie ulegają zerwaniu. Powstają nowe wiązania, tworząc cząsteczki dwutlenku węgla (CO2) i wody (H2O). Drewno i tlen to substraty, a dwutlenek węgla i woda to produkty.
Równania reakcji chemicznych: Język chemii
Równania reakcji chemicznych to sposób na zapisanie reakcji chemicznej za pomocą symboli i wzorów chemicznych. To tak, jakbyś miał przepis na ciasto, tylko zamiast składników używasz symboli pierwiastków i wzorów chemicznych związków. Równanie pokazuje, jakie substraty reagują ze sobą i jakie produkty powstają. Strzałka w równaniu wskazuje kierunek reakcji (od substratów do produktów).
Najprostszy przykład: 2H2 + O2 → 2H2O. Co to oznacza? Dwie cząsteczki wodoru (H2) reagują z jedną cząsteczką tlenu (O2), tworząc dwie cząsteczki wody (H2O). Liczby przed wzorami chemicznymi (zwane współczynnikami stechiometrycznymi) wskazują, ile cząsteczek każdego substratu i produktu bierze udział w reakcji. Ważne jest, aby równanie reakcji chemicznej było zbilansowane, czyli żeby liczba atomów każdego pierwiastka była taka sama po obu stronach równania.
Balansowanie równań reakcji chemicznych
Balansowanie równań reakcji chemicznych jest kluczowe, ponieważ odzwierciedla zasadę zachowania masy. Oznacza to, że atomy nie powstają ani nie znikają podczas reakcji chemicznej, tylko zmieniają swoje ułożenie. Dlatego liczba atomów każdego pierwiastka musi być taka sama po obu stronach równania.
Spróbujmy zbilansować równanie reakcji chemicznej spalania metanu: CH4 + O2 → CO2 + H2O. Po lewej stronie mamy 1 atom węgla, 4 atomy wodoru i 2 atomy tlenu. Po prawej stronie mamy 1 atom węgla, 2 atomy wodoru i 3 atomy tlenu. Widzimy, że liczba atomów wodoru i tlenu nie jest taka sama po obu stronach równania. Musimy dodać współczynniki stechiometryczne, aby to naprawić.
Zacznijmy od zbilansowania wodoru. Po lewej stronie mamy 4 atomy wodoru, a po prawej stronie tylko 2. Dlatego dodajemy współczynnik 2 przed wzorem H2O: CH4 + O2 → CO2 + 2H2O. Teraz mamy 4 atomy wodoru po obu stronach równania. Następnie, zbilansujmy tlen. Po lewej stronie mamy 2 atomy tlenu, a po prawej stronie mamy 4 atomy tlenu (2 w CO2 i 2 w 2H2O). Dodajemy współczynnik 2 przed wzorem O2: CH4 + 2O2 → CO2 + 2H2O. Teraz mamy 4 atomy tlenu po obu stronach równania. Sprawdzamy węgiel. Mamy 1 atom po obu stronach.
Ostatecznie otrzymujemy zbilansowane równanie reakcji chemicznej: CH4 + 2O2 → CO2 + 2H2O. Oznacza to, że jedna cząsteczka metanu reaguje z dwoma cząsteczkami tlenu, tworząc jedną cząsteczkę dwutlenku węgla i dwie cząsteczki wody.
Praktyczne zastosowania
Zrozumienie łączenia się atomów i równań reakcji chemicznych ma ogromne znaczenie w wielu dziedzinach nauki i technologii. Od projektowania nowych leków i materiałów, po optymalizację procesów przemysłowych i rozwiązywanie problemów środowiskowych. Wiedza o tym, jak atomy łączą się ze sobą i jak zachodzą reakcje chemiczne, pozwala nam tworzyć nowe technologie, ulepszać istniejące i lepiej rozumieć świat wokół nas. Na przykład, tworzenie nawozów, produkcja plastików, rozwój ogniw fotowoltaicznych, a nawet gotowanie, to tylko niektóre przykłady wykorzystania tych zasad.
Mam nadzieję, że ten artykuł pomógł Ci zrozumieć podstawowe zasady łączenia się atomów i równań reakcji chemicznych. Pamiętaj, że chemia to fascynująca dziedzina, która pozwala nam lepiej zrozumieć świat wokół nas. Im więcej się uczysz, tym więcej możliwości odkrywasz!