Woda jest niezwykłą substancją. Jest niezbędna do życia. Pokrywa około 71% powierzchni Ziemi.
Jej unikalne właściwości wynikają z jej struktury molekularnej. Pojedyncza cząsteczka wody (H₂O) składa się z dwóch atomów wodoru. Są one połączone z jednym atomem tlenu.
Atom tlenu jest bardziej elektroujemny niż atom wodoru. To znaczy, że silniej przyciąga elektrony. Powoduje to nierównomierne rozłożenie ładunku w cząsteczce wody. Strona z atomem tlenu ma ładunek częściowo ujemny (δ-), a strony z atomami wodoru mają ładunek częściowo dodatni (δ+). To czyni wodę cząsteczką polarną.
Roztwory Wodne
Roztwór to jednorodna mieszanina dwóch lub więcej substancji. Składa się z rozpuszczalnika i substancji rozpuszczonej. Rozpuszczalnik jest składnikiem występującym w większej ilości. Substancja rozpuszczona jest składnikiem występującym w mniejszej ilości.
W roztworach wodnych woda jest rozpuszczalnikiem. Roztwory wodne są bardzo powszechne. Wiele substancji dobrze rozpuszcza się w wodzie. Należą do nich sole, cukry, kwasy i zasady. Istnieją też substancje, które rozpuszczają się w wodzie słabo, np. tłuszcze.
Proces Rozpuszczania
Rozpuszczanie to proces, w którym substancja przechodzi do roztworu. Cząsteczki rozpuszczalnika otaczają cząsteczki substancji rozpuszczonej. To powoduje rozerwanie wiązań między cząsteczkami substancji rozpuszczonej. Powoduje to także rozproszenie cząsteczek substancji rozpuszczonej w rozpuszczalniku. Woda, jako rozpuszczalnik polarny, bardzo dobrze rozpuszcza związki jonowe i polarne.
Na przykład, gdy rozpuszczamy sól kuchenną (NaCl) w wodzie, cząsteczki wody otaczają jony sodu (Na⁺) i jony chlorkowe (Cl⁻). W wyniku tego jony te zostają oderwane od kryształu soli i rozpraszają się w wodzie. Proces ten nazywa się hydratacją jonów.
Rodzaje Roztworów Wodnych
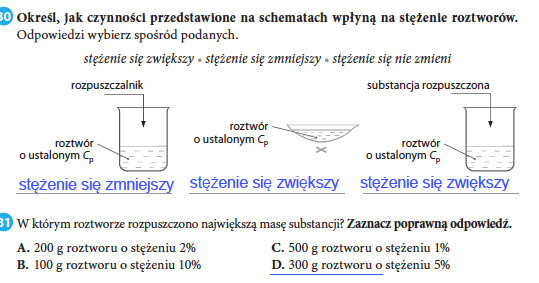
Roztwory wodne można klasyfikować na różne sposoby. Jednym ze sposobów jest klasyfikacja ze względu na stężenie substancji rozpuszczonej. Wyróżniamy roztwory rozcieńczone i stężone.
Roztwór rozcieńczony zawiera małą ilość substancji rozpuszczonej w stosunku do rozpuszczalnika. Roztwór stężony zawiera dużą ilość substancji rozpuszczonej w stosunku do rozpuszczalnika. Możemy także mieć roztwór nasycony. Roztwór nasycony to taki roztwór, w którym w danej temperaturze nie można już rozpuścić więcej substancji.
Innym sposobem klasyfikacji roztworów wodnych jest klasyfikacja ze względu na przewodnictwo elektryczne. Wyróżniamy elektrolity i nieelektrolity.
Elektrolity to substancje, których roztwory wodne przewodzą prąd elektryczny. Dzieje się tak, ponieważ elektrolity dysocjują na jony w wodzie. Do elektrolitów należą kwasy, zasady i sole. Nieelektrolity to substancje, których roztwory wodne nie przewodzą prądu elektrycznego. Nieelektrolity nie dysocjują na jony w wodzie. Do nieelektrolitów należą np. cukry i alkohol.
Właściwości Roztworów Wodnych
Roztwory wodne mają różne właściwości fizyczne i chemiczne. Te właściwości zależą od rodzaju i stężenia substancji rozpuszczonej. Niektóre z ważnych właściwości roztworów wodnych to: ciśnienie osmotyczne, obniżenie prężności pary i podwyższenie temperatury wrzenia.
Ciśnienie osmotyczne to ciśnienie, jakie należy przyłożyć do roztworu, aby zapobiec przepływowi rozpuszczalnika przez błonę półprzepuszczalną do roztworu. Obniżenie prężności pary to obniżenie prężności pary rozpuszczalnika nad roztworem w porównaniu z czystym rozpuszczalnikiem. Podwyższenie temperatury wrzenia to podwyższenie temperatury wrzenia roztworu w porównaniu z czystym rozpuszczalnikiem. Te właściwości są znane jako właściwości koligatywne. Zależą one tylko od liczby cząsteczek substancji rozpuszczonej, a nie od jej rodzaju.
Zastosowania Roztworów Wodnych
Roztwory wodne mają szerokie zastosowanie w różnych dziedzinach. Są wykorzystywane w przemyśle chemicznym, medycynie, rolnictwie i życiu codziennym.
W przemyśle chemicznym roztwory wodne są wykorzystywane jako rozpuszczalniki, reagenty i katalizatory. W medycynie roztwory wodne są wykorzystywane jako leki, płyny infuzyjne i środki dezynfekcyjne. W rolnictwie roztwory wodne są wykorzystywane jako nawozy i pestycydy. W życiu codziennym roztwory wodne są wykorzystywane do gotowania, sprzątania i higieny osobistej.
Na przykład, roztwór soli fizjologicznej (0,9% roztwór NaCl) jest szeroko stosowany w medycynie jako płyn infuzyjny. Roztwory octu (kwas octowy w wodzie) są używane jako środek czyszczący i konserwujący żywność. Roztwory mydła i detergentów są używane do sprzątania i higieny osobistej. Roztwory nawozów (np. roztwór saletry amonowej) są stosowane w rolnictwie do nawożenia roślin.
Zrozumienie właściwości wody i roztworów wodnych jest kluczowe w wielu dziedzinach nauki i technologii. Dzięki temu możemy lepiej wykorzystywać te substancje w różnych zastosowaniach i rozwiązywać problemy związane z ich użytkowaniem.