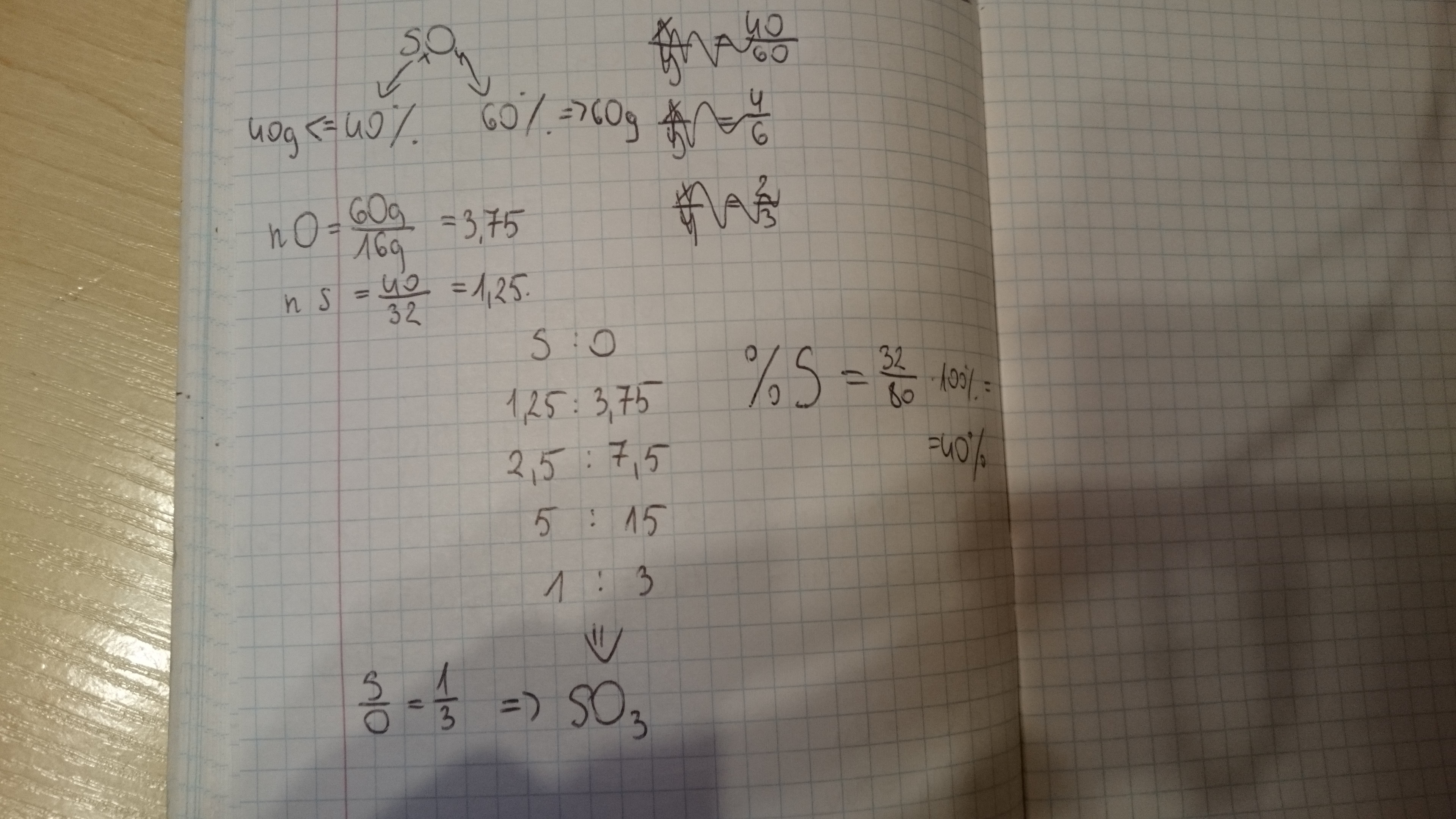Zadanie brzmi: W pewnym tlenku siarki zawartość procentowa siarki wynosi 50.
Musimy ustalić wzór empiryczny tego tlenku.
Co to jest tlenek siarki?
Tlenki siarki to związki chemiczne składające się z siarki i tlenu.
Istnieje kilka różnych tlenków siarki, takich jak dwutlenek siarki (SO2) i trójtlenek siarki (SO3).
Analiza procentowa
Mamy podaną zawartość procentową siarki, która wynosi 50%. Oznacza to, że w 100 gramach związku znajduje się 50 gramów siarki.
Reszta, czyli 100% - 50% = 50%, to zawartość tlenu. Zatem w 100 gramach związku znajduje się 50 gramów tlenu.
Przeliczenie na mole
Musimy przeliczyć masy siarki i tlenu na liczbę moli. Użyjemy do tego mas molowych tych pierwiastków.
Masa molowa siarki (S) wynosi około 32 g/mol.
Masa molowa tlenu (O) wynosi około 16 g/mol.
Obliczanie moli siarki
Liczba moli siarki = masa siarki / masa molowa siarki.
Liczba moli siarki = 50 g / 32 g/mol ≈ 1.56 mola.
Obliczanie moli tlenu
Liczba moli tlenu = masa tlenu / masa molowa tlenu.
Liczba moli tlenu = 50 g / 16 g/mol ≈ 3.125 mola.
Ustalanie stosunku molowego
Teraz musimy ustalić stosunek molowy siarki do tlenu. Dzielimy obie wartości przez mniejszą z nich (czyli liczbę moli siarki).
Stosunek molowy S : O = 1.56 mola : 3.125 mola.
Dzielimy obie wartości przez 1.56:
Stosunek molowy S : O ≈ 1 : 2.
Wzór empiryczny
Stosunek molowy siarki do tlenu wynosi 1:2. Oznacza to, że na jeden atom siarki przypadają dwa atomy tlenu.
Zatem wzór empiryczny tego tlenku siarki to SO2 (dwutlenek siarki).
Weryfikacja
Sprawdźmy, czy zawartość procentowa siarki w SO2 wynosi 50%.
Masa molowa SO2 = masa molowa S + 2 * masa molowa O.
Masa molowa SO2 ≈ 32 g/mol + 2 * 16 g/mol = 32 g/mol + 32 g/mol = 64 g/mol.
Zawartość procentowa siarki w SO2 = (masa molowa S / masa molowa SO2) * 100%.
Zawartość procentowa siarki w SO2 ≈ (32 g/mol / 64 g/mol) * 100% = 0.5 * 100% = 50%.
Wynik się zgadza. Zatem szukany tlenek siarki to SO2.
Podsumowanie
Znaleźliśmy wzór empiryczny tlenku siarki, w którym zawartość procentowa siarki wynosi 50%. Jest to dwutlenek siarki (SO2).
Proces obliczeniowy polegał na:
- Wyznaczeniu zawartości procentowej tlenu.
- Przeliczeniu gramów siarki i tlenu na mole.
- Ustaleniu stosunku molowego siarki do tlenu.
- Określeniu wzoru empirycznego na podstawie stosunku molowego.
- Weryfikacji wyniku poprzez obliczenie zawartości procentowej siarki we wzorze empirycznym.
Ten proces jest stosowany do określania wzorów empirycznych innych związków chemicznych na podstawie ich analizy elementarnej.