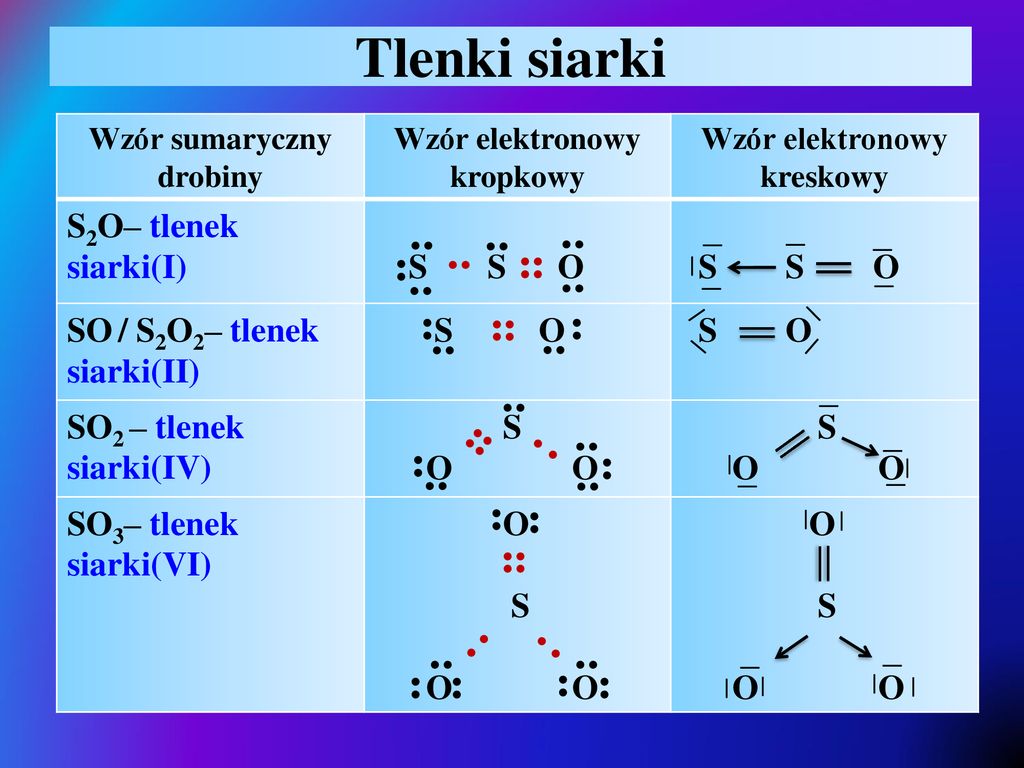
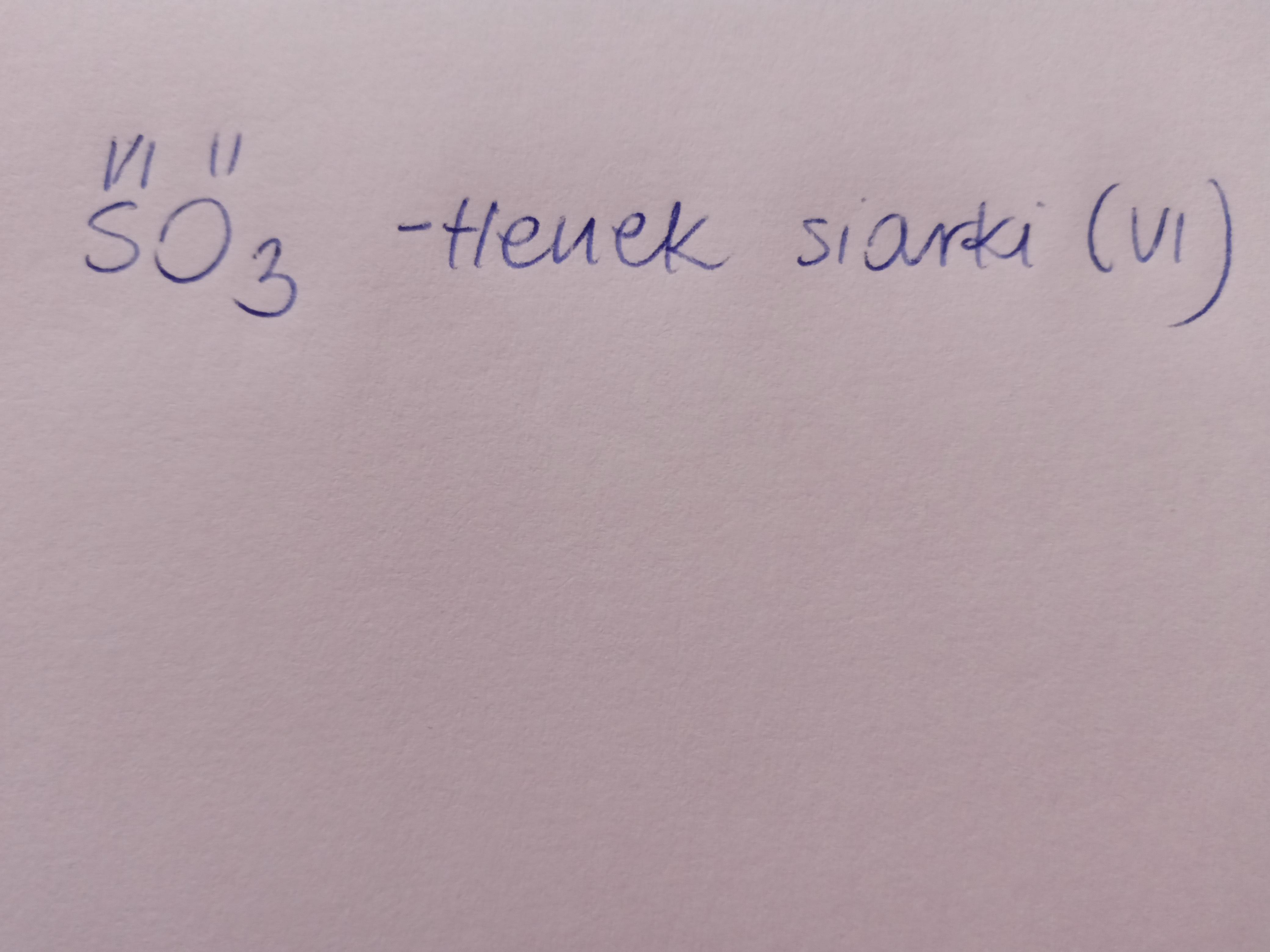Zajmiemy się teraz Tlenkiem Siarki(VI). Ciekawi Cię jego wzór sumaryczny? Już go poznasz! To SO3.
Spróbujmy go zrozumieć wizualnie. Wyobraź sobie klocki LEGO. Jeden klocek to atom Siarki (S). Potrzebujemy go jednego.
Kolejne trzy klocki to atomy Tlenu (O). Musimy je wszystkie połączyć z klockiem siarki. Wtedy powstanie nasza cząsteczka SO3!
Budowa cząsteczki SO3
Spójrzmy na to dokładniej. Siarka jest w centrum. Otaczają ją trzy atomy Tlenu. Pomyśl o Siarkę jako o słońcu. A o Tlenach jako o planetach krążących wokół niego.
Każde połączenie Siarki z Tlenem to wiązanie. W SO3 są trzy takie wiązania. Każde wiązanie to jak most między dwoma atomami.
Atomy Tlenu trzymają się mocno Siarki. To jak magnesy przyciągające się do siebie.
Dlaczego (VI)?
Zauważasz rzymską liczbę (VI)? To ważna informacja. Oznacza stopień utlenienia Siarki.
Pomyśl o stopniach utlenienia jak o mocy. Siarka w SO3 ma moc 6. Oznacza to, ile elektronów "oddała" (w pewnym sensie) atomom Tlenu.
Tlen jest bardziej "chciwy" na elektrony niż Siarka. Dlatego Siarka oddaje mu elektrony. Przez to Siarka zyskuje ładunek dodatni (+6), a Tlen ujemny.
Właściwości i zastosowania SO3
SO3 to bezbarwna ciecz. W normalnych warunkach występuje w postaci stałej. A dokładnie tworzy kryształy o wyglądzie igieł.
Bardzo burzliwie reaguje z wodą! Wyobraź sobie, że wrzucasz kostkę lodu do rozgrzanego oleju. Podobna reakcja!
Powstaje wtedy Kwas Siarkowy (H2SO4). Czyli bardzo silny kwas.
Dlatego też, SO3 używa się do produkcji Kwasu Siarkowego. Ten kwas jest bardzo ważny w przemyśle.
Wyobraź sobie fabrykę nawozów. Tam Kwas Siarkowy jest niezbędny. Podobnie w produkcji detergentów. Albo barwników.
SO3 ma też inne zastosowania. Używa się go do sulfonowania związków organicznych. Brzmi skomplikowanie?
Chodzi o to, że dodaje się grupę SO3H do innych związków. To zmienia ich właściwości. Tak powstają np. niektóre leki.
SO3 a środowisko
Niestety, SO3 może być szkodliwy dla środowiska. Powstaje np. podczas spalania paliw zawierających siarkę.
SO3 reaguje z wodą w atmosferze. Tworzy Kwas Siarkowy. A to prowadzi do kwaśnych deszczy.
Kwaśne deszcze niszczą lasy. Zakwaszają glebę. Szkodzą roślinom i zwierzętom wodnym. Dlatego ważne jest ograniczanie emisji SO3.
Porównaj to do dymu z komina. Jeśli dym zawiera SO3, to szkodzi środowisku. Trzeba więc używać filtrów, żeby go oczyścić.
Podsumowanie
Tlenek Siarki(VI), wzór sumaryczny SO3. Pamiętaj o tym wzorze!
Pamiętaj, że Siarka jest w centrum, otoczona przez trzy Tleny. Stopień utlenienia Siarki wynosi +6.
SO3 reaguje z wodą. Tworzy Kwas Siarkowy. Używany w przemyśle, ale szkodliwy dla środowiska, jeśli dostanie się do atmosfery.
Teraz już wiesz więcej o SO3! Gratulacje!