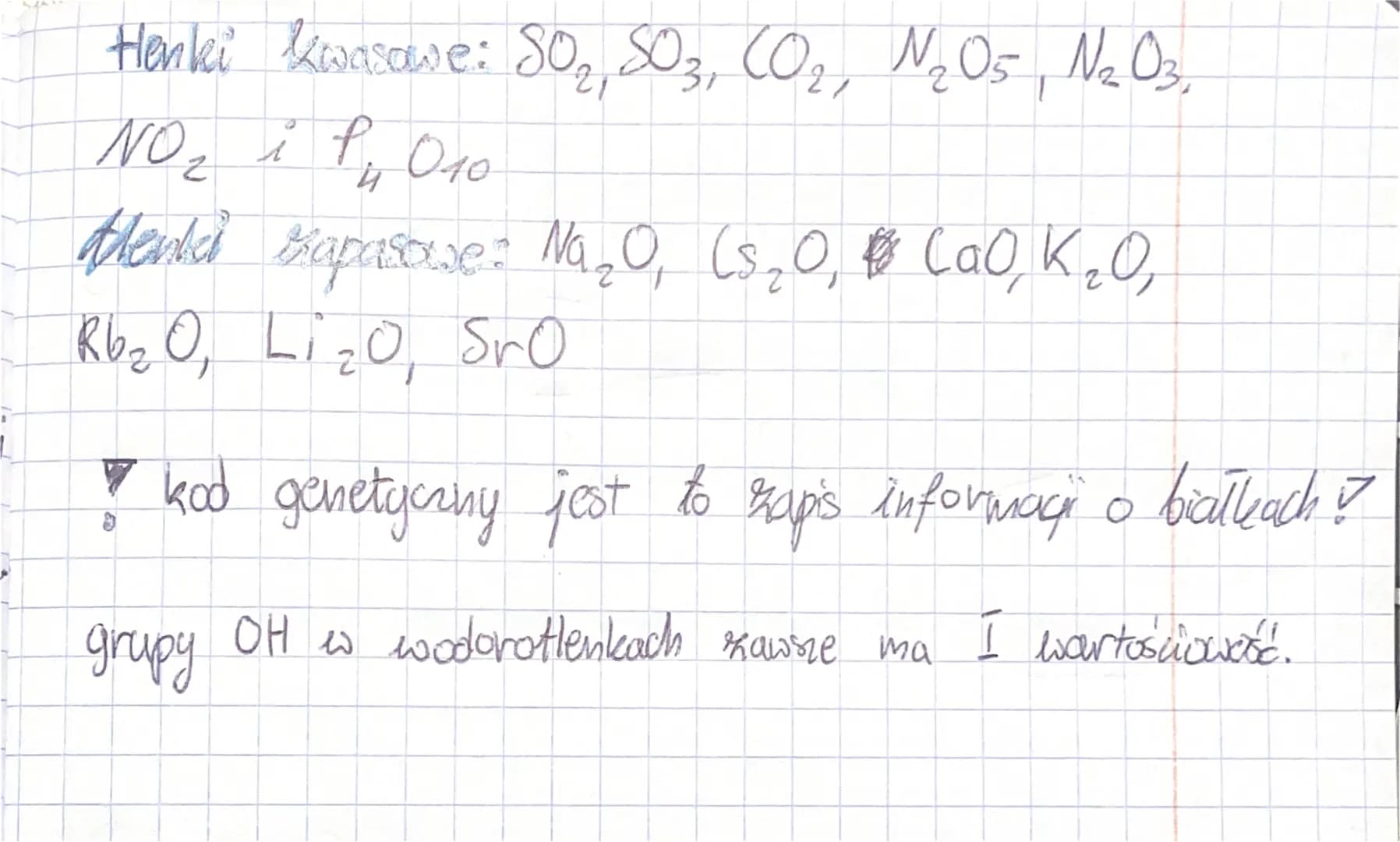Chemia bywa trudna, ale zrozumienie tlenków, wodorotlenków, kwasów i soli to podstawa. Wyobraź sobie, że to jak składniki przepisu na chemiczne danie!
Tlenki: Tlen i ktoś jeszcze
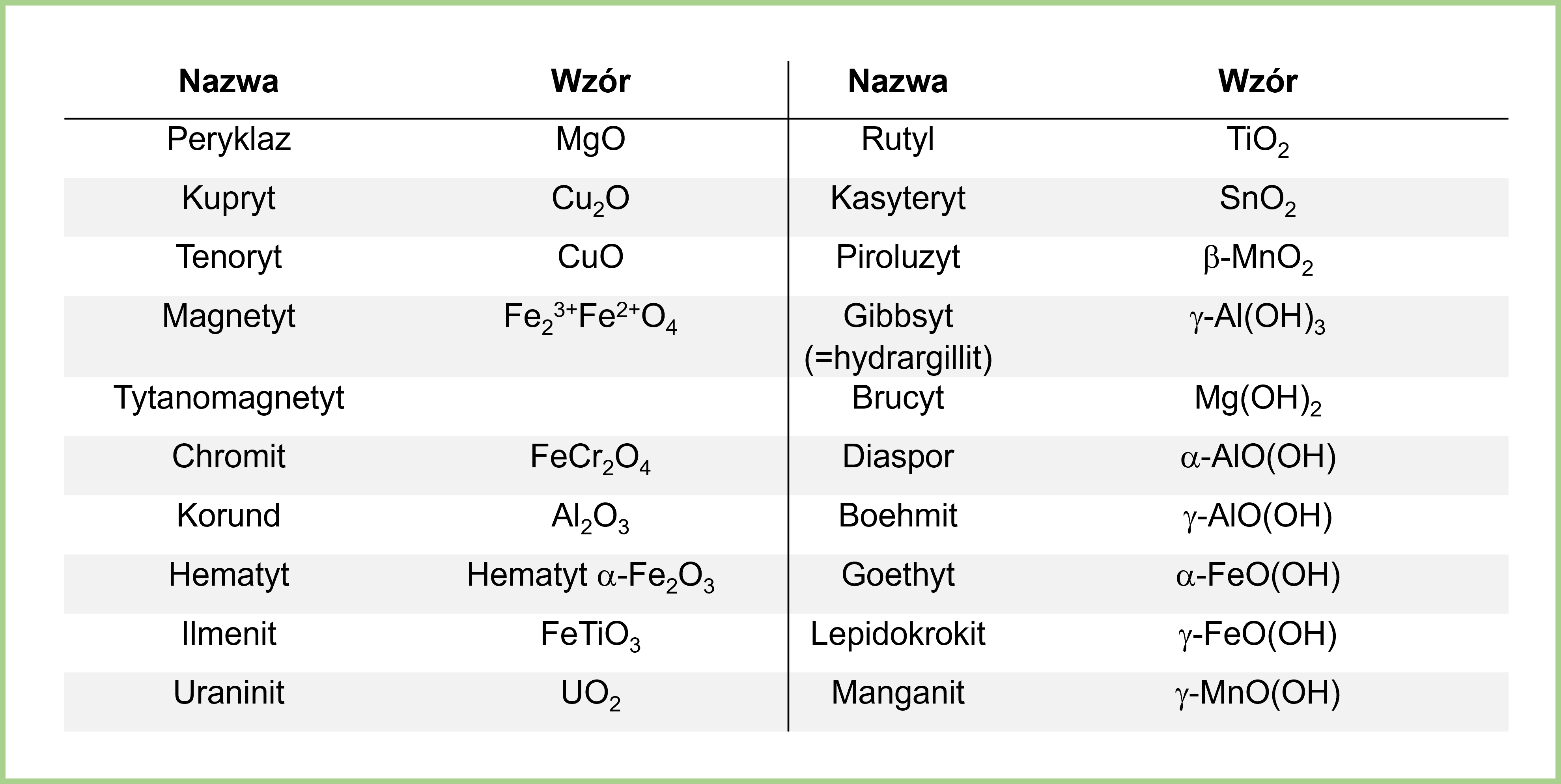
Tlenki to związki tlenu z innym pierwiastkiem. Pomyśl o rdzy na metalu. To tlenek żelaza! Tlen (O) połączył się z żelazem (Fe) i powstało Fe₂O₃.
Mamy różne rodzaje tlenków. Podział zależy od ich zachowania w wodzie.
Tlenki kwasowe
Tlenki kwasowe, jak SO₂ (dwutlenek siarki), reagują z wodą dając kwasy. Wyobraź sobie dym unoszący się z komina, który miesza się z deszczem. Powstaje kwaśny deszcz!
Dla wizualnych: wyobraź sobie tlenek kwasowy jako małego chemika, który wrzuca do wody odczynnik i mówi: "Teraz będzie kwaśno!"
Tlenki zasadowe
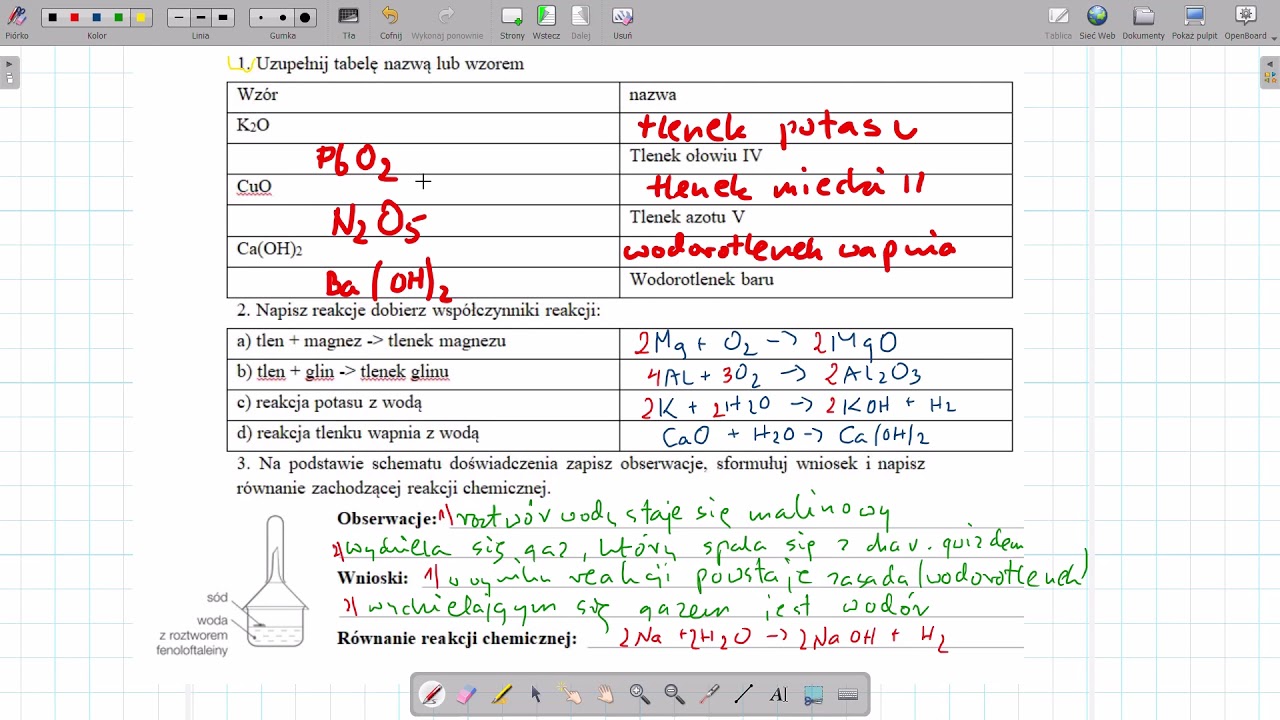
Tlenki zasadowe, np. CaO (tlenek wapnia), reagują z wodą dając zasady (wodorotlenki). Tlenek wapnia, znany jako wapno palone, stosuje się w budownictwie.
Pomyśl o tlenku zasadowym jako o budowniczym, który miesza tlenek z wodą, aby stworzyć mocną zaprawę - zasadę.
Tlenki obojętne
Tlenki obojętne, np. CO (tlenek węgla), nie reagują ani z kwasami, ani z zasadami. Są neutralne. To taki obserwator, który stoi z boku i niczego nie zmienia.
Wyobraź sobie, że to jak woda – nie jest ani kwaśna, ani zasadowa, po prostu jest.
Wodorotlenki: Metal i grupa OH
Wodorotlenki to związki metalu z grupą hydroksylową (OH). Najprościej: metal + OH.
Na przykład: NaOH (wodorotlenek sodu) – popularna zasada, znana również jako soda kaustyczna. Używana do udrażniania rur.
Wizualizacja: Wyobraź sobie metal jako silnego rycerza, a grupę OH jako jego tarczę. Razem tworzą wodorotlenek.
Wodorotlenki są zasadami. Oznacza to, że mają pH powyżej 7.
Kwasy: Dają jony H+
Kwasy to związki, które w roztworze wodnym oddają jony wodorowe (H⁺). Im więcej jonów H⁺, tym mocniejszy kwas.
Przykład: HCl (kwas solny). To mocny kwas, obecny w żołądku, który pomaga trawić jedzenie.
Wizualizacja: Wyobraź sobie kwas jako kogoś, kto chętnie oddaje innym swoje "plusy" (H⁺). Im więcej plusów odda, tym jest bardziej "kwaśny".
Kwasy mają pH poniżej 7.
Kwasy beztlenowe
Kwasy beztlenowe, np. HCl (kwas chlorowodorowy), składają się z wodoru i niemetalu. Nie zawierają tlenu.
Kwasy tlenowe
Kwasy tlenowe, np. H₂SO₄ (kwas siarkowy), zawierają wodór, tlen i niemetal.
Sole: Kwas + Zasada = Sól + Woda
Sole powstają w wyniku reakcji kwasu z zasadą (reakcja zobojętniania). Produktami tej reakcji są sól i woda.
Przykład: NaCl (chlorek sodu), czyli sól kuchenna. Powstaje z reakcji HCl (kwas solny) i NaOH (wodorotlenek sodu).
Wizualizacja: Wyobraź sobie kwas i zasadę jako dwie osoby, które się kłócą. Kiedy się godzą, powstaje sól – coś stabilnego i przydatnego.
HCl + NaOH → NaCl + H₂O
Sól składa się z kationu (dodatnio naładowanego jonu) pochodzącego od zasady i anionu (ujemnie naładowanego jonu) pochodzącego od kwasu.
Różne kwasy i zasady dają różne sole. Mamy sole tlenowe i beztlenowe, w zależności od tego, czy kwas użyty do reakcji zobojętniania był tlenowy, czy beztlenowy.
Sole mogą być obojętne, kwaśne lub zasadowe, w zależności od tego, jakie kwasy i zasady użyto do ich otrzymania.
Zrozumienie tlenków, wodorotlenków, kwasów i soli to klucz do chemicznych tajemnic. Pamiętaj o wizualizacjach i przykładach z życia codziennego. Powodzenia na sprawdzianie!