Zacznijmy naszą przygodę z kwasami karboksylowymi. Są one bardzo ważne w chemii organicznej i występują w wielu miejscach wokół nas.
Co to są Kwasy Karboksylowe?
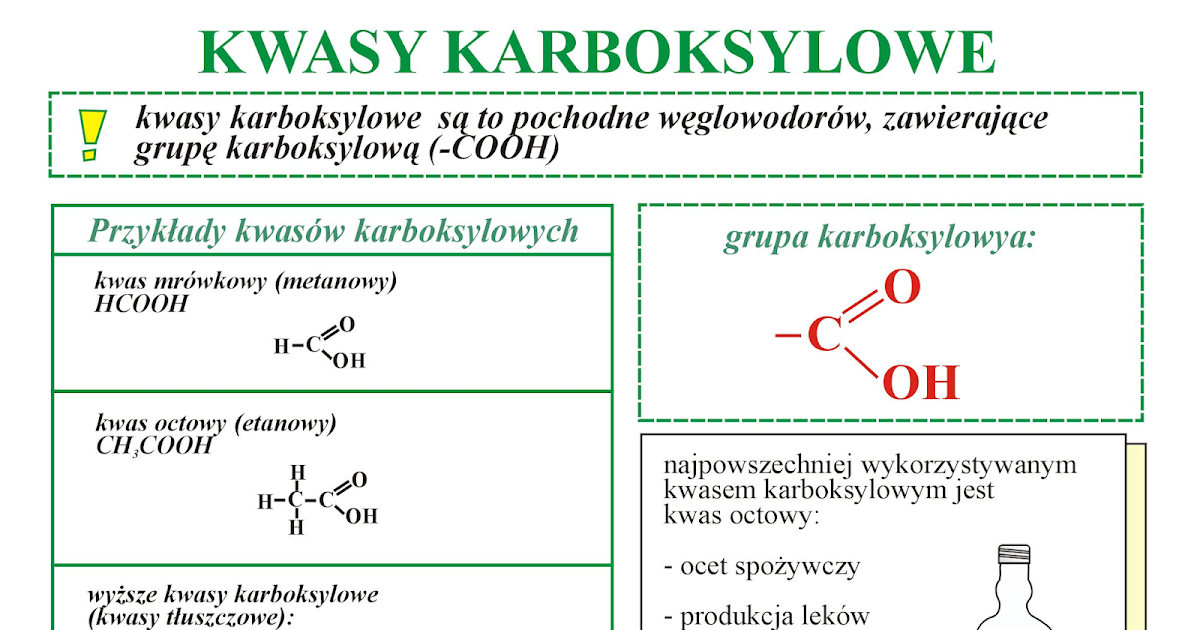
Kwasy karboksylowe to związki organiczne, które w swojej strukturze zawierają grupę funkcyjną zwaną grupą karboksylową. Grupę tę zapisujemy jako -COOH. Składa się ona z grupy karbonylowej (C=O) i grupy hydroksylowej (-OH), połączonych z tym samym atomem węgla. To właśnie obecność tej grupy decyduje o właściwościach kwasowych tych związków.
Wzór ogólny kwasów karboksylowych to R-COOH, gdzie R oznacza grupę alkilową lub arylową. Grupa alkilowa to łańcuch węglowodorowy, na przykład metyl (CH3) lub etyl (C2H5). Grupa arylowa to pierścień aromatyczny, na przykład fenyl (C6H5).
Przykłady Kwasów Karboksylowych
Najprostszym kwasem karboksylowym jest kwas metanowy, znany również jako kwas mrówkowy. Jego wzór to HCOOH. Jest on obecny w jadzie mrówek, stąd jego nazwa. Kwas mrówkowy ma charakterystyczny, ostry zapach.
Kolejnym przykładem jest kwas etanowy, popularnie nazywany kwasem octowym. Jego wzór to CH3COOH. Jest to główny składnik octu spożywczego. Ocet, którego używamy w kuchni, to roztwór kwasu octowego w wodzie.
Kwas propionowy (C2H5COOH) i kwas butanowy (C3H7COOH), zwany również kwasem masłowym, to kolejne przykłady. Kwas masłowy ma nieprzyjemny zapach, charakterystyczny dla zjełczałego masła.
Właściwości Kwasów Karboksylowych
Kwasy karboksylowe mają charakterystyczne właściwości, które wynikają z obecności grupy karboksylowej. Są to związki polarne, co oznacza, że mają wyraźny biegun dodatni i ujemny. Ta polarność wpływa na ich rozpuszczalność w wodzie.
Krótkie łańcuchy węglowodorowe (np. kwas mrówkowy, octowy, propionowy) dobrze rozpuszczają się w wodzie. Długie łańcuchy węglowodorowe (np. kwas stearynowy) są mniej rozpuszczalne w wodzie. Wynika to z faktu, że długi łańcuch węglowodorowy jest hydrofobowy (odpycha wodę).
Kwasy karboksylowe reagują z zasadami, tworząc sole i wodę. Ta reakcja nazywana jest reakcją neutralizacji. Na przykład, kwas octowy reaguje z wodorotlenkiem sodu (NaOH), tworząc octan sodu (CH3COONa) i wodę (H2O). Reakcja ta neutralizuje kwas, czyli zmniejsza jego kwasowość.
Otrzymywanie Kwasów Karboksylowych
Istnieje kilka metod otrzymywania kwasów karboksylowych. Jedną z nich jest utlenianie alkoholi. Pierwszorzędowe alkohole (czyli takie, w których grupa -OH jest połączona z węglem związanym z jednym innym węglem) mogą być utleniane do aldehydów, a następnie do kwasów karboksylowych.
Inną metodą jest hydroliza estrów. Estry to związki powstające w reakcji kwasu karboksylowego z alkoholem. Hydroliza estru, czyli jego reakcja z wodą, prowadzi do odtworzenia kwasu karboksylowego i alkoholu.
Można też otrzymać kwasy karboksylowe poprzez karboksylację związków Grignarda. To bardziej zaawansowana metoda, stosowana w chemii organicznej, ale warto o niej wspomnieć.
Zastosowanie Kwasów Karboksylowych
Kwasy karboksylowe mają bardzo szerokie zastosowanie. Kwas octowy jest używany w przemyśle spożywczym jako konserwant i dodatek smakowy. Jest także wykorzystywany w produkcji tworzyw sztucznych, włókien syntetycznych i leków.
Kwas benzoesowy jest używany jako konserwant w żywności i kosmetykach. Jego sole, takie jak benzoesan sodu, również znajdują zastosowanie jako konserwanty.
Wyższe kwasy karboksylowe, takie jak kwas stearynowy i kwas palmitynowy, są składnikami mydeł i detergentów. Są także wykorzystywane w produkcji kosmetyków i smarów.
Kwasy karboksylowe są również ważne w procesach biologicznych. Aminokwasy, które budują białka, zawierają grupę karboksylową. Kwasy tłuszczowe, które są składnikami tłuszczów, również należą do kwasów karboksylowych.
Podsumowując, kwasy karboksylowe to niezwykle ważna grupa związków organicznych. Znajdują one zastosowanie w wielu dziedzinach naszego życia, od przemysłu spożywczego po medycynę. Zrozumienie ich budowy, właściwości i reakcji jest kluczowe dla zrozumienia chemii organicznej.