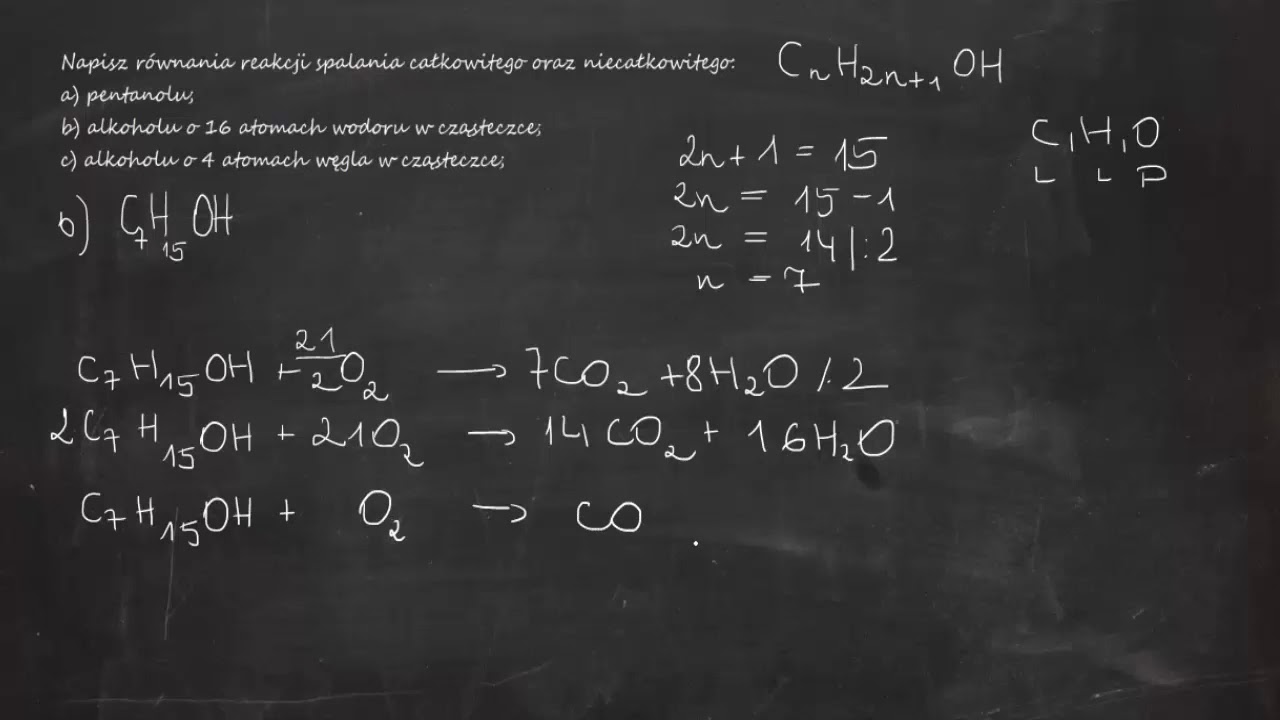Hej! Zastanawiałeś się kiedyś, co się dzieje, kiedy coś się pali? To nie tylko magiczny ogień! Za tym wszystkim kryją się reakcje chemiczne. Dzisiaj skupimy się na spalaniu pentanolu, a konkretnie na jego dwóch rodzajach: spalaniu całkowitym i niecałkowitym. Przygotuj się na fascynującą podróż do świata chemii!
Czym jest spalanie?
Spalanie to szybka reakcja chemiczna, która zachodzi między substancją palną a utleniaczem, zazwyczaj tlenem. Ta reakcja wydziela ciepło i światło. Pomyśl o zapalonej świeczce albo ognisku. To właśnie spalanie! Reakcja zachodzi, ponieważ atomy i molekuły przemieszczają się i tworzą nowe wiązania. To bardzo energetyczny proces.
Kluczowym elementem jest obecność paliwa – substancji, która się pali, i utleniacza – substancji, która umożliwia spalanie. Bez jednego z tych składników, ogień nie powstanie. Najczęściej utleniaczem jest tlen z powietrza. W spalaniu zawsze powstają nowe produkty, inne niż pierwotne.
Pentanol – nasz bohater
Teraz poznajmy naszego bohatera – pentanol. To alkohol, czyli związek organiczny zawierający grupę hydroksylową (-OH). Jego wzór chemiczny to C5H12O. Pentanol jest cieczą bezbarwną i ma charakterystyczny zapach.
Istnieje kilka izomerów pentanolu, czyli związków o tym samym wzorze sumarycznym, ale różnej budowie. Są to np. pentan-1-ol, pentan-2-ol i pentan-3-ol. Wszystkie one ulegają spalaniu, ale w tym artykule będziemy mówić o pentanolu ogólnie. Pamiętaj, że to paliwo w naszej reakcji spalania. Będzie reagował z tlenem.
Spalanie całkowite pentanolu
Spalanie całkowite to idealny scenariusz. W tym procesie, pentanol reaguje z dużą ilością tlenu. Produkty, które powstają, to dwutlenek węgla (CO2) i woda (H2O). To najefektywniejszy sposób spalania, ponieważ uwalnia najwięcej energii.
Możemy to zapisać za pomocą równania reakcji: C5H12O + 7.5 O2 → 5 CO2 + 6 H2O Zauważ, że po obu stronach równania mamy tę samą liczbę atomów każdego pierwiastka. To jest zbilansowane równanie chemiczne. W spalaniu całkowitym otrzymujemy tylko dwutlenek węgla i wodę.
Wyobraź sobie, że masz idealnie wyregulowany palnik gazowy w laboratorium. Dostarczasz do niego odpowiednią ilość gazu i bardzo dużo tlenu. Płomień jest czysty, niebieski, a spalanie przebiega efektywnie. To jest przykład spalania całkowitego. Jest to najbardziej pożądane spalanie, gdyż zyskujemy najwięcej energii przy najmniejszej emisji zanieczyszczeń.
Spalanie niecałkowite pentanolu
Spalanie niecałkowite to sytuacja, gdy brakuje tlenu. Wtedy reakcja spalania nie przebiega w pełni. Oprócz dwutlenku węgla i wody, powstają inne produkty, takie jak tlenek węgla (CO), węgiel (C), a czasami nawet inne związki organiczne.
Spalanie niecałkowite jest mniej efektywne energetycznie niż spalanie całkowite. Dodatkowo, produkty spalania niecałkowitego mogą być szkodliwe dla środowiska i zdrowia. Tlenek węgla jest trujący, a cząstki węgla (sadza) zanieczyszczają powietrze.
Przykładowe równania reakcji spalania niecałkowitego (jest ich wiele, w zależności od ilości tlenu): C5H12O + 5 O2 → 2 CO2 + 3 CO + 6 H2O (powstaje CO) C5H12O + 3 O2 → 5 C + 6 H2O (powstaje węgiel – sadza)
Pomyśl o starym piecu węglowym, który dymi czarnym dymem. To jest przykład spalania niecałkowitego. Brakuje tlenu, więc węgiel spala się nieefektywnie, tworząc sadzę i tlenek węgla. Czarny dym to właśnie niespalony węgiel. Spalanie niecałkowite jest niepożądane.
Różnice między spalaniem całkowitym a niecałkowitym
Podsumujmy różnice między spalaniem całkowitym i niecałkowitym: Spalanie całkowite wymaga dużej ilości tlenu, a produktami są dwutlenek węgla i woda. Jest efektywne energetycznie i stosunkowo czyste. Z kolei Spalanie niecałkowite zachodzi przy niedoborze tlenu, a produktami są dwutlenek węgla, woda, tlenek węgla i węgiel (sadza). Jest mniej efektywne energetycznie i zanieczyszcza środowisko.
Kluczowym czynnikiem decydującym o rodzaju spalania jest dostępność tlenu. Im więcej tlenu, tym większa szansa na spalanie całkowite. Regulacja dopływu powietrza do pieca czy silnika spalinowego jest kluczowa dla efektywnego i czystego spalania. Pamiętaj, że dążymy do spalania całkowitego.
Przykłady z życia codziennego
Gdzie możemy zaobserwować spalanie pentanolu lub innych alkoholi w życiu codziennym? Paliwo w silnikach spalinowych to mieszanka różnych związków, w tym alkoholi. Proces spalania w silniku powinien być jak najbardziej zbliżony do spalania całkowitego, aby zapewnić efektywność i minimalizować emisję zanieczyszczeń. Dlatego konstruktorzy silników starają się zapewnić optymalną mieszankę paliwa i powietrza.
Palniki spirytusowe, używane np. w turystyce, spalają alkohol (często denaturat, zawierający etanol). Jeśli palnik jest dobrze wyregulowany, spalanie jest zbliżone do całkowitego. Jednak przy niedostatecznym dopływie powietrza, może dojść do spalania niecałkowitego, co objawia się żółtym płomieniem i sadzą. Obserwuj kolor płomienia! Niebieski płomień oznacza spalanie całkowite.
W przemyśle chemicznym, pentanol i inne alkohole są używane jako rozpuszczalniki i substraty w różnych reakcjach. Spalanie jest czasem wykorzystywane do utylizacji odpadów organicznych, ale zawsze pod ścisłą kontrolą, aby zapewnić jak najmniejszą emisję szkodliwych substancji. Kontrola spalania przemysłowego jest bardzo ważna dla środowiska.
Podsumowanie
Mam nadzieję, że teraz rozumiesz różnicę między spalaniem całkowitym a niecałkowitym pentanolu. Pamiętaj, że spalanie całkowite to idealny scenariusz, w którym powstaje dwutlenek węgla i woda. Natomiast spalanie niecałkowite zachodzi przy niedoborze tlenu i prowadzi do powstawania szkodliwych substancji, takich jak tlenek węgla i sadza. Zrozumienie tego procesu jest kluczowe dla wielu dziedzin, od chemii po inżynierię środowiska. Powodzenia w dalszej nauce!