Cześć! Chcesz zrozumieć równania reakcji chemicznych? Super! Zaraz wszystko stanie się jasne. Wyobraź sobie, że gotujesz.
Potrzebujesz składników, prawda? To tak jak substraty w reakcji chemicznej.
Na końcu masz gotowe danie – to produkty.
A przepis? To właśnie równanie reakcji!
Co to jest Równanie Reakcji?
Równanie reakcji to taki chemiczny "przepis". Pokazuje, co reaguje z czym (substraty) i co powstaje (produkty).
Używamy symboli chemicznych, np. H2O na wodę.
Strzałka (→) pokazuje kierunek reakcji: od substratów do produktów.
Przykład: H2 + O2 → H2O
Dlaczego Musimy Bilansować Równania?
Wyobraź sobie, że masz ciasto. Nie możesz nagle "stworzyć" mąki z niczego, prawda? Wszystko musi się zgadzać.
W chemii też tak jest! Prawo zachowania masy mówi, że atomy nie giną i nie powstają w reakcji. One się tylko przegrupowują.
Dlatego musimy bilansować równania. Musimy dopasować liczby atomów po obu stronach strzałki.
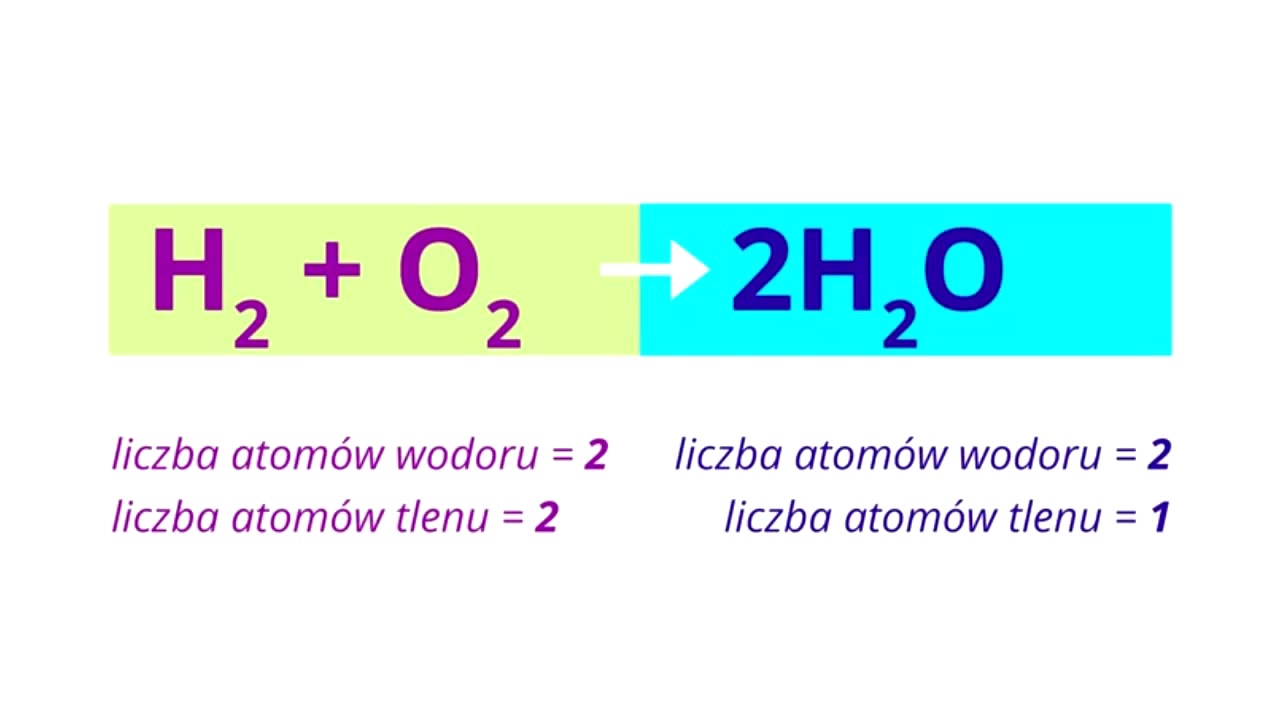
Spójrz na nasz przykład: H2 + O2 → H2O. Nie jest zbilansowane!
Po lewej stronie (substraty) mamy 2 atomy wodoru (H) i 2 atomy tlenu (O).
Po prawej stronie (produkt) mamy 2 atomy wodoru (H) i tylko 1 atom tlenu (O).
Brakuje tlenu! Musimy to naprawić.
Jak Bilansować Równania?
Najprościej? Metodą prób i błędów. Trochę jak układanie puzzli.
Krok 1: Zapisz równanie: H2 + O2 → H2O
Krok 2: Sprawdź, co się nie zgadza. W naszym przypadku – tlen.
Krok 3: Dodaj współczynniki (liczby przed wzorami chemicznymi). Nigdy nie zmieniaj wzorów samych w sobie! To tak, jakbyś zmieniał składniki ciasta w trakcie pieczenia.
Spróbujmy dodać "2" przed H2O: H2 + O2 → 2 H2O
Teraz mamy 2 atomy tlenu po obu stronach (super!). Ale... wodoru mamy teraz 4 po prawej (2 x 2 = 4), a tylko 2 po lewej.
Krok 4: Poprawiamy! Dodajmy "2" przed H2: 2 H2 + O2 → 2 H2O
Teraz mamy 4 atomy wodoru i 2 atomy tlenu po obu stronach. Bingo! Równanie jest zbilansowane.
Inny Przykład: Spalanie Metanu
Metan (CH4) to główny składnik gazu ziemnego. Używamy go do gotowania i ogrzewania.
Podczas spalania metan reaguje z tlenem (O2), tworząc dwutlenek węgla (CO2) i wodę (H2O).
Równanie reakcji (niezbilansowane): CH4 + O2 → CO2 + H2O
Zbilansujmy je krok po kroku:
Krok 1: Widzimy, że węgiel (C) jest zbilansowany (1 atom po obu stronach).
Krok 2: Sprawdzamy wodór (H). Mamy 4 atomy po lewej i tylko 2 po prawej. Dodajemy "2" przed H2O: CH4 + O2 → CO2 + 2 H2O
Krok 3: Teraz wodór jest zbilansowany. Sprawdzamy tlen (O). Mamy 2 atomy po lewej i 4 po prawej (2 z CO2 i 2 z 2 H2O).
Krok 4: Dodajemy "2" przed O2: CH4 + 2 O2 → CO2 + 2 H2O
Teraz wszystko się zgadza! Równanie jest zbilansowane: CH4 + 2 O2 → CO2 + 2 H2O
Dlaczego to Ważne?
Bilansowanie równań to podstawa stechiometrii – działu chemii, który zajmuje się ilościowymi relacjami w reakcjach. Dzięki niemu możemy obliczyć, ile substratu potrzebujemy, żeby otrzymać daną ilość produktu.
To przydatne w laboratorium, w przemyśle, a nawet w kuchni! Wyobraź sobie, że chcesz przygotować większą porcję ciasta. Musisz znać proporcje składników, prawda?
Podsumowanie:
- Równanie reakcji to chemiczny przepis.
- Substraty to składniki, produkty to wynik reakcji.
- Bilansowanie zapewnia, że atomy się nie "znikają".
- Używamy współczynników, żeby zbilansować równania.
Ćwicz, a szybko staniesz się mistrzem bilansowania! Powodzenia!
![Zapisywanie równań reakcji chemicznej #7 [ Reakcje chemiczne ] - YouTube Równania Reakcji Chemicznych Przykłady I Rozwiązania](https://margaretweigel.com/storage/img/zapisywanie-rownan-reakcji-chemicznej-7-reakcje-chemiczne-youtube-6842b616c1f6d.jpg)