Witaj! Przygotuj się na powtórkę z reszt kwasowych i ich wartościowości. To ważny temat, a ja pomogę Ci go zrozumieć krok po kroku!
Czym są reszty kwasowe?
Reszty kwasowe to fragmenty cząsteczek kwasów, które powstają po oderwaniu od nich atomów wodoru.
Pomyśl o kwasie jak o całości. Reszta kwasowa to to, co zostaje, gdy "zabierzemy" wodór.
Na przykład, od kwasu chlorowodorowego (HCl) odrywamy jeden atom wodoru (H). Powstaje reszta kwasowa chlorkowa (Cl).
Kluczowe jest zrozumienie, że reszty kwasowe zawsze posiadają ładunek ujemny.
Wartościowość reszt kwasowych
Wartościowość reszty kwasowej to liczba atomów wodoru, które zostały oderwane od cząsteczki kwasu.
Inaczej mówiąc, to ilość ujemnych ładunków, które posiada dana reszta.
Pamiętaj, wartościowość reszty kwasowej informuje nas, ile wiązań może utworzyć ta reszta z innymi atomami lub grupami atomów.
Im więcej atomów wodoru oderwano od kwasu, tym wyższa jest wartościowość reszty.
Przykłady wartościowości
Kwas chlorowodorowy (HCl): Odrwany 1 atom wodoru. Reszta kwasowa chlorkowa (Cl) jest jednowartościowa.
Kwas siarkowy (VI) (H2SO4): Odrwane 2 atomy wodoru. Reszta kwasowa siarczanowa(VI) (SO4) jest dwuwartościowa.
Kwas ortofosforowy (V) (H3PO4): Odrwane 3 atomy wodoru. Reszta kwasowa ortofosforanowa(V) (PO4) jest trójwartościowa.
Jak ustalić wartościowość reszty kwasowej?
Najprostszy sposób to policzenie atomów wodoru, które zawiera kwas.
Liczba atomów wodoru w kwasie równa się wartościowości reszty kwasowej.
Spójrz na wzór kwasu. Pod indeksem wodoru znajdziesz potrzebną informację.
Jeżeli kwas to HX, to reszta kwasowa X jest jednowartościowa.
Jeżeli kwas to H2X, to reszta kwasowa X jest dwuwartościowa.
Jeżeli kwas to H3X, to reszta kwasowa X jest trójwartościowa.
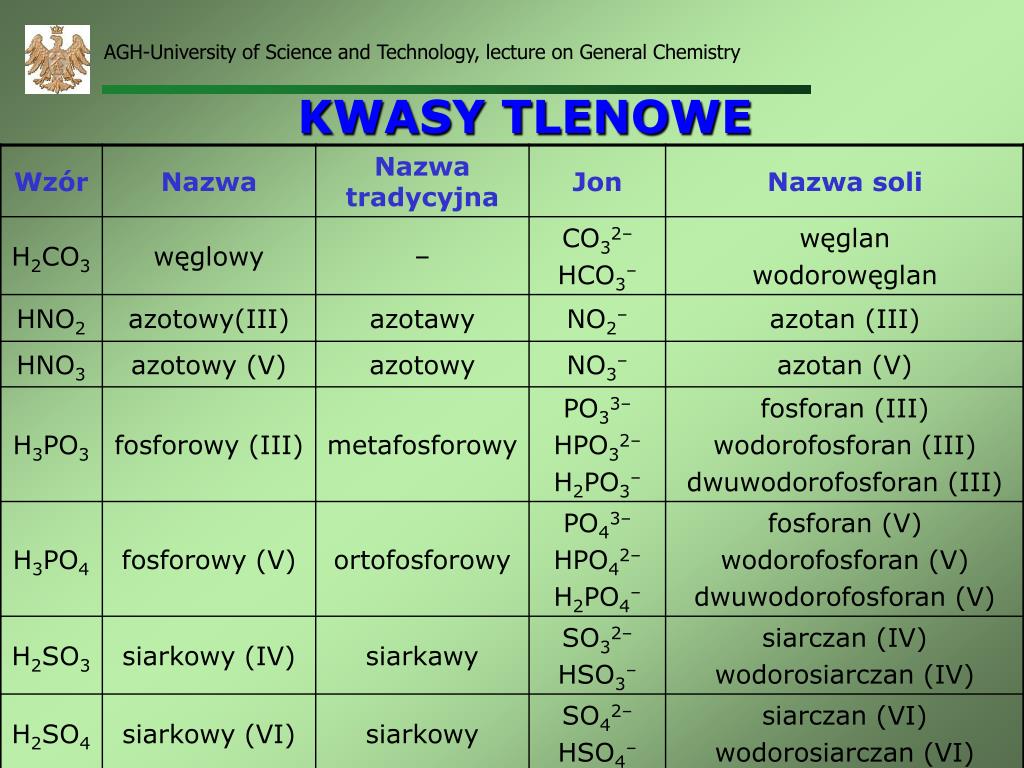
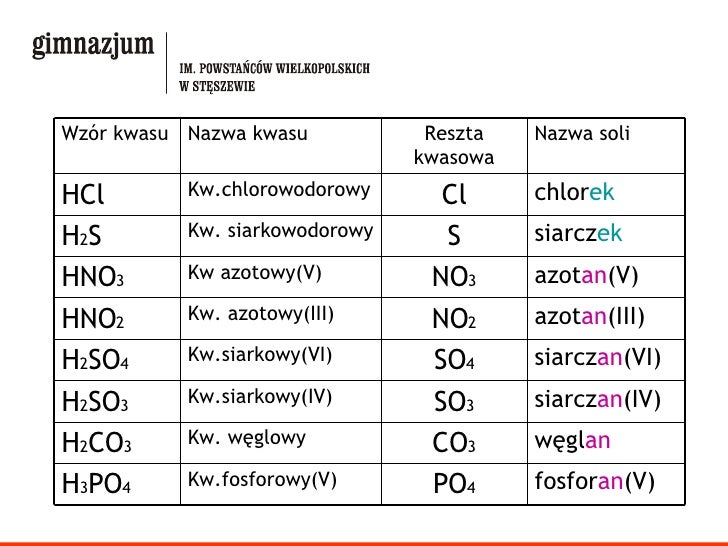
Najważniejsze reszty kwasowe i ich wartościowości
Warto znać kilka popularnych reszt kwasowych:
- Chlorkowa (Cl-): Powstaje od HCl. Wartościowość: 1.
- Azotanowa(V) (NO3-): Powstaje od HNO3. Wartościowość: 1.
- Siarczanowa(VI) (SO42-): Powstaje od H2SO4. Wartościowość: 2.
- Siarczanowa(IV) (SO32-): Powstaje od H2SO3. Wartościowość: 2.
- Węglanowa (CO32-): Powstaje od H2CO3. Wartościowość: 2.
- Ortofosforanowa(V) (PO43-): Powstaje od H3PO4. Wartościowość: 3.
Zwróć uwagę na ładunek reszty kwasowej. Informuje on o wartościowości!
Zastosowanie wiedzy o resztach kwasowych
Znajomość reszt kwasowych i ich wartościowości jest niezbędna do poprawnego pisania wzorów sumarycznych i strukturalnych soli.
Sole składają się z kationu metalu (lub jonu amonowego) i anionu, którym jest reszta kwasowa.
Aby napisać poprawny wzór soli, musisz "skrzyżować" wartościowości metalu i reszty kwasowej.
Na przykład, chlorek wapnia (CaCl2): Wapń (Ca) jest dwuwartościowy, chlorek (Cl) jest jednowartościowy. Dlatego potrzebujemy dwóch jonów chlorkowych, aby zrównoważyć ładunek wapnia.
Pamiętaj, że wiedza o resztach kwasowych jest fundamentem chemii nieorganicznej!
Przykładowe zadania
Spróbuj rozwiązać te zadania:
- Jaka jest wartościowość reszty kwasowej w kwasie azotowym(III) (HNO2)?
- Napisz wzór sumaryczny siarczanu(VI) glinu. (Glin jest trójwartościowy).
- Podaj nazwę reszty kwasowej, która powstaje od kwasu węglowego (H2CO3).
Podsumowanie
Reszty kwasowe to fragmenty kwasów po oderwaniu atomów wodoru.
Wartościowość reszty kwasowej to liczba oderwanych atomów wodoru.
Wartościowość jest równa liczbie ujemnych ładunków reszty kwasowej.
Znajomość reszt kwasowych jest kluczowa do pisania wzorów soli!
Mam nadzieję, że ta powtórka była pomocna. Powodzenia na egzaminie! Pamiętaj, dasz radę!