Cześć! Dziś nauczymy się przyporządkowywać nazwy węglowodorów ich wzorom. Brzmi skomplikowanie? Spokojnie, rozłożymy to na czynniki pierwsze. Zobaczycie, że to całkiem proste!
Czym są Węglowodory?
Zacznijmy od podstaw. Węglowodory to związki organiczne, które składają się tylko i wyłącznie z dwóch pierwiastków: węgla (C) i wodoru (H). Są wszędzie wokół nas! Na przykład, gaz ziemny, którym ogrzewamy domy, to głównie metan, który jest najprostszym węglowodorem.
Dlatego nazwa: "węglo-wodo-ry". Węgiel plus wodór. Łatwe, prawda? Różnią się one między sobą liczbą atomów węgla i wodoru oraz sposobem, w jaki te atomy są ze sobą połączone. To właśnie te różnice wpływają na ich właściwości.
Podział Węglowodorów
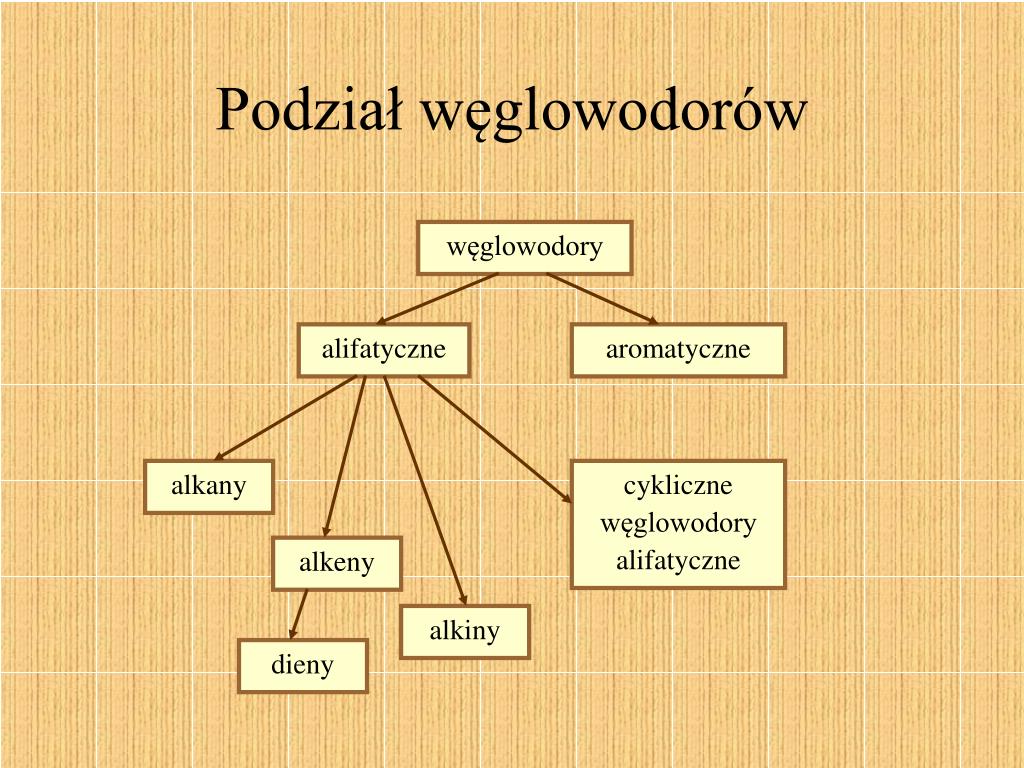
Węglowodory dzielimy na różne grupy, a najważniejsze z nich to: alkany, alkeny, alkiny i węglowodory aromatyczne. Każda z tych grup ma swoje charakterystyczne cechy i wzory ogólne. Poznajmy je po kolei.
Alkany
Alkany to najprostsza grupa węglowodorów. W ich cząsteczkach występują tylko wiązania pojedyncze między atomami węgla. To oznacza, że każdy atom węgla jest połączony z innymi atomami węgla i wodoru tylko jedną "linią".
Wzór ogólny alkanów to CnH2n+2, gdzie "n" oznacza liczbę atomów węgla w cząsteczce. Przykładowo, jeśli mamy alkan z 3 atomami węgla (n=3), to liczba atomów wodoru będzie wynosić 2*3 + 2 = 8. Zatem wzór takiego alkanu to C3H8. Jest to propan, gaz używany np. w kuchenkach turystycznych.
Nazwy alkanów tworzymy dodając końcówkę -an do rdzenia, który wskazuje na liczbę atomów węgla. Najprostsze alkany to: metan (CH4), etan (C2H6), propan (C3H8), butan (C4H10) i pentan (C5H12). Pamiętaj, że metan to główny składnik gazu ziemnego.
Alkeny
Alkeny to węglowodory, w których występuje co najmniej jedno wiązanie podwójne między atomami węgla. To oznacza, że dwa atomy węgla są połączone dwiema "liniami". Obecność wiązania podwójnego wpływa na właściwości chemiczne alkenów - są bardziej reaktywne niż alkany.
Wzór ogólny alkenów to CnH2n, gdzie "n" to liczba atomów węgla. Zauważ, że alkeny mają mniej atomów wodoru niż alkany o tej samej liczbie atomów węgla. Przykładowo, alken z 2 atomami węgla (n=2) ma wzór C2H4. Jest to eten (etylen), wykorzystywany np. do produkcji plastiku.
Nazwy alkenów tworzymy dodając końcówkę -en do rdzenia wskazującego na liczbę atomów węgla. Najprostsze alkeny to: eten (C2H4), propen (C3H6), buten (C4H8) i penten (C5H10). Pamiętaj, wiązanie podwójne musi znajdować się pomiędzy atomami węgla.
Alkiny
Alkiny to węglowodory, które zawierają co najmniej jedno wiązanie potrójne między atomami węgla. Czyli dwa atomy węgla są połączone trzema "liniami". Wiązanie potrójne jest jeszcze silniejsze i krótsze niż wiązanie podwójne, co sprawia, że alkiny są jeszcze bardziej reaktywne.
Wzór ogólny alkinów to CnH2n-2. Widzimy, że alkiny mają jeszcze mniej atomów wodoru niż alkeny o tej samej liczbie atomów węgla. Alkin z 2 atomami węgla (n=2) ma wzór C2H2. Jest to etyn (acetylen), używany np. w palnikach spawalniczych.
Nazwy alkinów tworzymy dodając końcówkę -in do rdzenia. Przykłady to: etyn (C2H2), propin (C3H4), butin (C4H6) i pentin (C5H8). Pamiętaj, że etyn, znany również jako acetylen, jest wykorzystywany do spawania.
Węglowodory Aromatyczne
Węglowodory aromatyczne to grupa węglowodorów o specyficznej strukturze pierścieniowej. Najbardziej znanym węglowodorem aromatycznym jest benzen (C6H6). Jego cząsteczka ma kształt sześciokąta, w którym występuje naprzemiennie wiązanie pojedyncze i podwójne pomiędzy atomami węgla. Te wiązania są zdelokalizowane, co nadaje mu szczególną stabilność i właściwości.
Węglowodory aromatyczne często mają charakterystyczny zapach (stąd nazwa "aromatyczne"). Są one składnikami wielu substancji, w tym leków, barwników i tworzyw sztucznych. Benzen jest podstawowym surowcem w przemyśle chemicznym.
Wzory ogólnego dla węglowodorów aromatycznych nie da się tak łatwo zapisać, ponieważ to zależy od rodzaju pierścienia i podstawników, które są do niego przyłączone. Najważniejsze to zapamiętać benzen (C6H6) i jego pochodne. Pochodne benzenu tworzy się zastępując atomy wodoru innymi grupami.
Podsumowanie
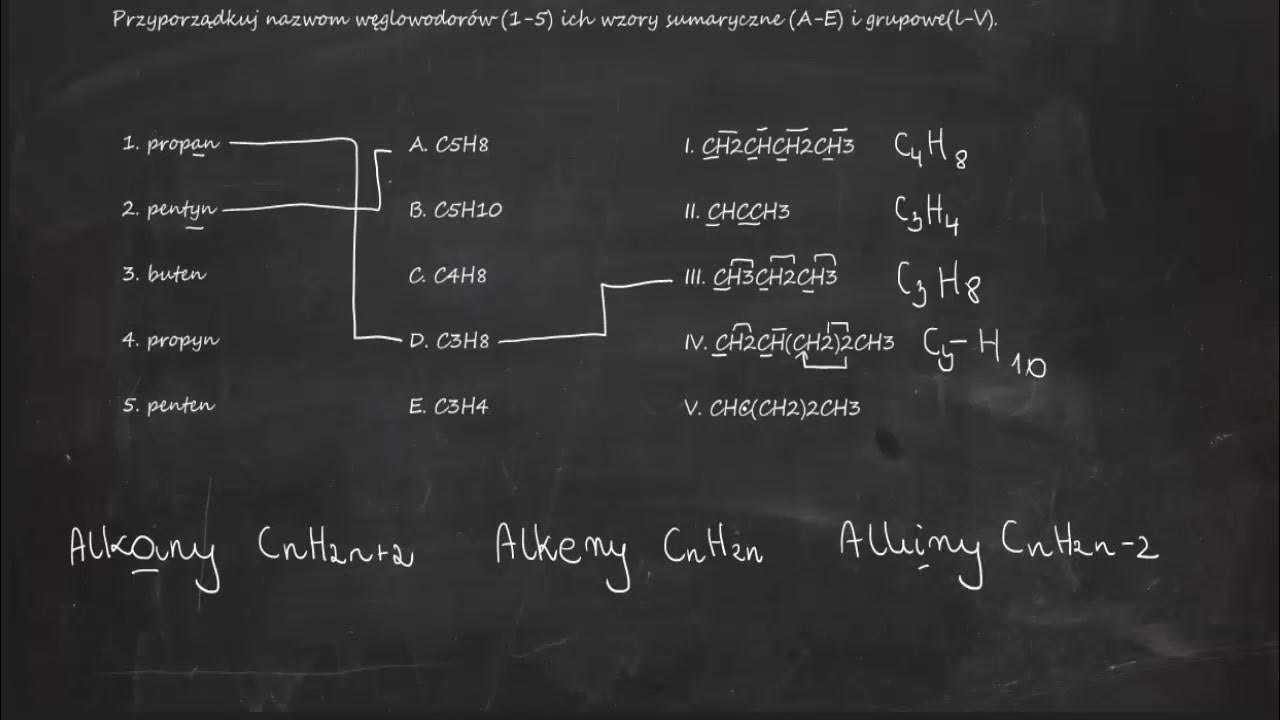
Zobaczmy jak to działa w praktyce! Spróbujmy przyporządkować wzory do nazw:
- Metan: CH4
- Etan: C2H6
- Propen: C3H6
- Butan: C4H10
- Etyn: C2H2
- Benzen: C6H6
Pamiętaj o końcówkach nazw i wzorach ogólnych. Ćwicz, a szybko opanujesz tę wiedzę. Powodzenia!