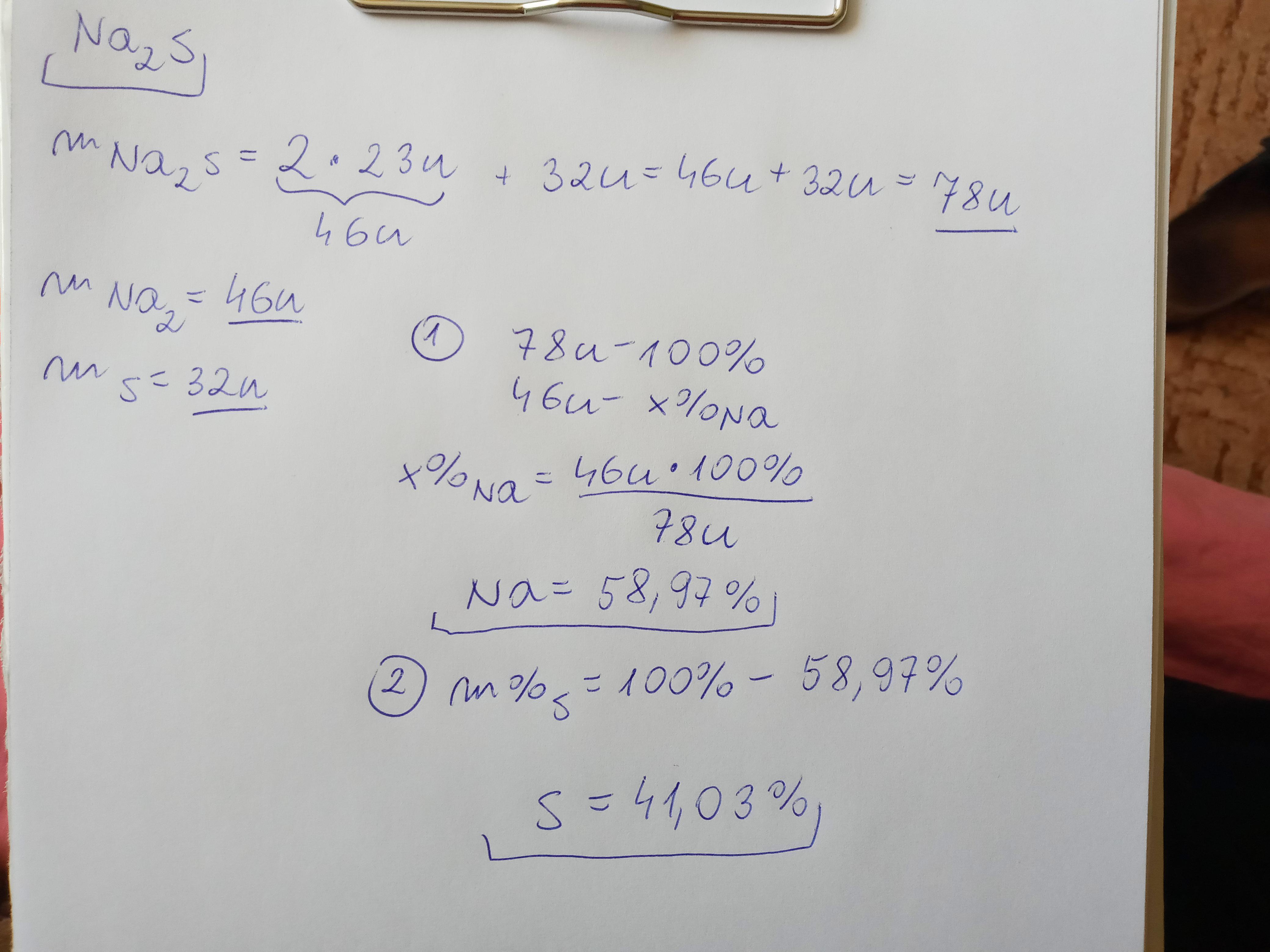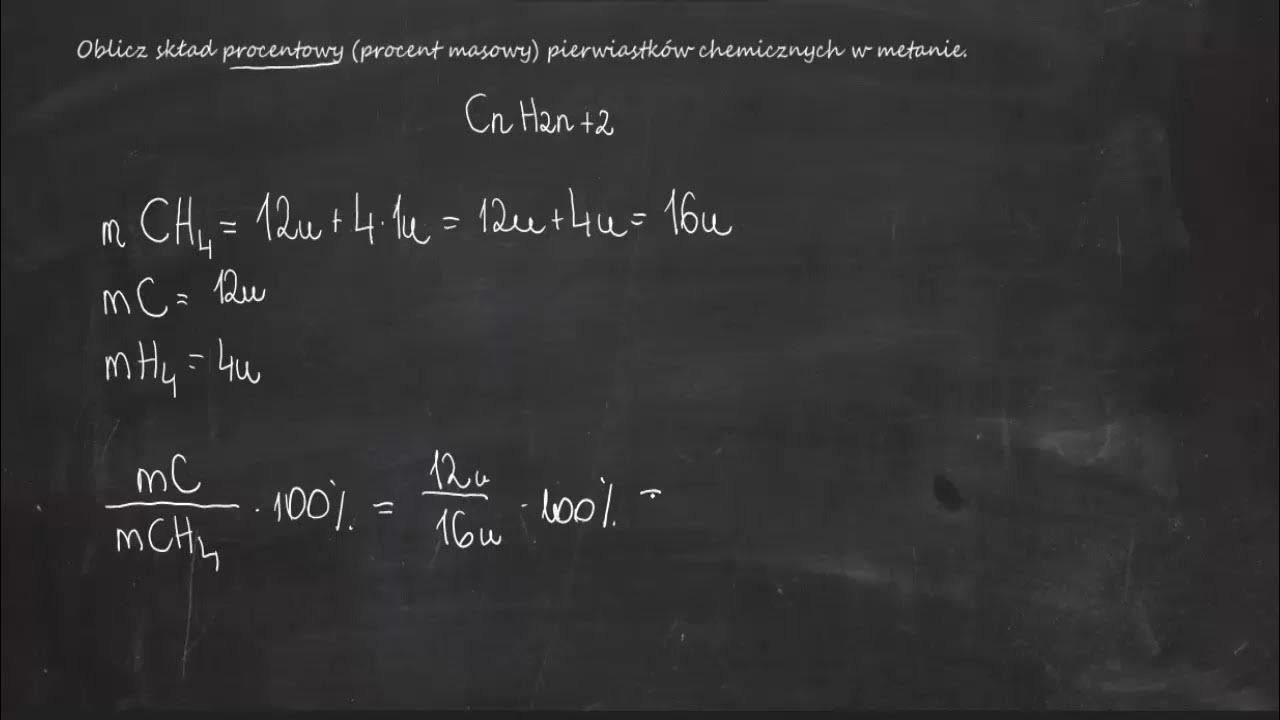Drogi Nauczycielu/Droga Nauczycielko,
Mam nadzieję, że ten artykuł okaże się pomocny w objaśnianiu zagadnienia obliczania składu procentowego, a konkretnie procentu masowego pierwiastków w związkach chemicznych, na przykładzie metanu (CH4). Celem jest przedstawienie tematu w sposób zrozumiały dla uczniów i zaprezentowanie metod, które ułatwią im przyswojenie tego zagadnienia.
Krok po Kroku: Obliczanie Składu Procentowego
1. Określenie Wzoru Sumarycznego Związku
Upewnij się, że uczniowie rozumieją, czym jest wzór sumaryczny związku. W przypadku metanu jest to CH4, co oznacza, że w jednej cząsteczce metanu znajduje się jeden atom węgla (C) i cztery atomy wodoru (H).
2. Obliczenie Masy Molowej Związku
Masa molowa związku to suma mas molowych wszystkich atomów wchodzących w jego skład. Aby to obliczyć, uczniowie potrzebują układu okresowego pierwiastków.
- Masa molowa węgla (C) ≈ 12,01 g/mol
- Masa molowa wodoru (H) ≈ 1,01 g/mol
Zatem masa molowa metanu (CH4) wynosi:
M(CH4) = 1 × M(C) + 4 × M(H) = (1 × 12,01) + (4 × 1,01) = 12,01 + 4,04 = 16,05 g/mol
Upewnij się, że uczniowie rozumieją, dlaczego mnożymy masę molową wodoru przez 4 – wynika to z obecności czterech atomów wodoru w cząsteczce metanu.
3. Obliczenie Procentu Masowego Każdego Pierwiastka
Procent masowy pierwiastka w związku to stosunek masy danego pierwiastka w jednej moli związku do masy molowej całego związku, wyrażony w procentach.
Procent masowy węgla (C) w CH4:
%C = (M(C) / M(CH4)) × 100% = (12,01 / 16,05) × 100% ≈ 74,83%
Procent masowy wodoru (H) w CH4:
%H = (4 × M(H) / M(CH4)) × 100% = (4 × 1,01 / 16,05) × 100% = (4,04 / 16,05) × 100% ≈ 25,17%
Sprawdzenie: %C + %H ≈ 74,83% + 25,17% = 100% (wynik powinien dać w przybliżeniu 100%, ewentualne różnice wynikają z zaokrągleń).
Typowe Błędy i Jak Im Zapobiegać
- Błąd: Pomijanie mnożenia masy molowej atomu przez jego liczbę w cząsteczce.
- Rozwiązanie: Podkreślaj znaczenie indeksów stechiometrycznych we wzorze sumarycznym. Ćwiczcie liczenie atomów każdego pierwiastka w różnych związkach.
- Błąd: Używanie złych wartości mas molowych.
- Rozwiązanie: Upewnij się, że uczniowie korzystają z aktualnej wersji układu okresowego i wiedzą, gdzie znaleźć masę molową. Zwróć uwagę na jednostki (g/mol).
- Błąd: Błędy w obliczeniach matematycznych.
- Rozwiązanie: Zachęcaj do sprawdzania obliczeń i używania kalkulatorów. Skup się na metodycznym podejściu do rozwiązywania zadań.
- Błąd: Nierozumienie definicji procentu masowego.
- Rozwiązanie: Wyjaśnij, że procent masowy to miara tego, jaką część masy całego związku stanowi masa danego pierwiastka. Porównaj to do obliczania procentu w innych sytuacjach, np. procentu oceny z testu.
Jak Uatrakcyjnić Lekcję?
- Praktyczne przykłady: Użyj związków, z którymi uczniowie mają styczność w życiu codziennym, np. woda (H2O), cukier (C12H22O11), sól kuchenna (NaCl). Poproś uczniów o odnalezienie składu różnych substancji z etykiet produktów.
- Gry i konkursy: Zorganizuj konkurs, w którym uczniowie będą rywalizować w obliczaniu składu procentowego różnych związków. Możesz użyć kart z wzorami związków i poprosić uczniów o jak najszybsze obliczenie procentu masowego wybranego pierwiastka.
- Wykorzystanie technologii: Skorzystaj z interaktywnych symulacji i kalkulatorów online, które pomogą uczniom wizualizować proces obliczania składu procentowego.
- Praca w grupach: Podziel uczniów na grupy i daj im do rozwiązania zadania o różnym stopniu trudności. Wspólna praca i dyskusja pomogą im lepiej zrozumieć materiał.
- Metoda analogii: Porównaj obliczanie procentu masowego do obliczania udziału procentowego w budżecie domowym. Na przykład, jeśli budżet domowy wynosi 1000 zł, a na jedzenie wydaje się 300 zł, to udział procentowy wydatków na jedzenie wynosi 30%.
- Zadania problemowe: Zaproponuj zadania, w których uczniowie będą musieli obliczyć skład procentowy, aby rozwiązać dany problem, np. "Który nawóz zawiera więcej azotu: azotan amonu (NH4NO3) czy mocznik (CO(NH2)2)?"
Podsumowanie
Obliczanie składu procentowego to fundamentalne zagadnienie w chemii, które wymaga od uczniów zrozumienia pojęć takich jak masa molowa, wzór sumaryczny i proporcje. Wykorzystując przedstawione wskazówki i uatrakcyjniając lekcję, możesz pomóc uczniom w skutecznym opanowaniu tego tematu. Pamiętaj, że kluczem jest cierpliwość, systematyczność i dostosowywanie metod nauczania do indywidualnych potrzeb uczniów.
Powodzenia w pracy!