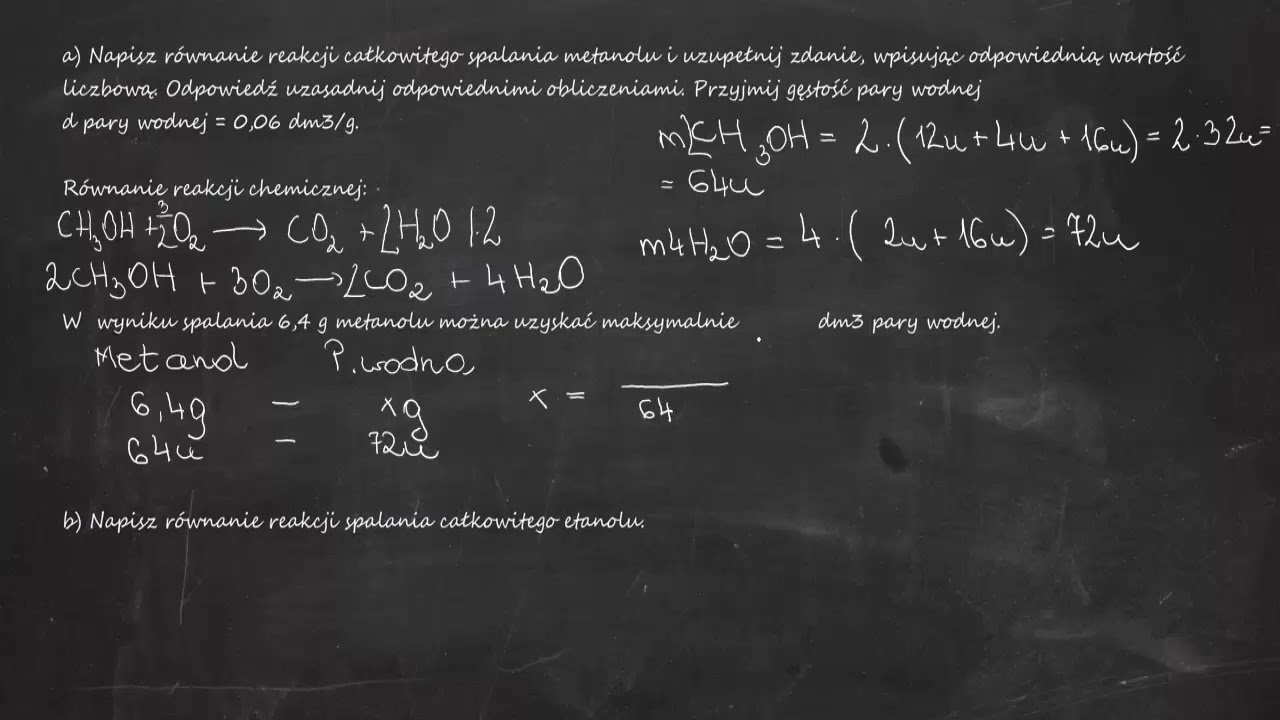Spalanie to bardzo ważny proces chemiczny.
Warto go dobrze rozumieć.
Czym jest spalanie?
Spalanie to reakcja chemiczna, w której substancja reaguje z utleniaczem, zazwyczaj z tlenem, wydzielając ciepło i światło.
Pomyśl o palącym się drewnie w kominku.
To właśnie spalanie!
Rodzaje spalania
Istnieją różne rodzaje spalania.
Rozróżniamy spalanie całkowite i niecałkowite.
Zaczniemy od wyjaśnienia podstawowych pojęć.
Spalanie całkowite
Spalanie całkowite zachodzi, gdy jest wystarczająca ilość tlenu.
Produktami spalania całkowitego są dwutlenek węgla (CO2) i woda (H2O).
Przykład: spalanie metanu (gazu ziemnego) w kuchence.
Równanie reakcji:
CH4 + 2O2 → CO2 + 2H2O
Spalanie niecałkowite
Spalanie niecałkowite zachodzi, gdy brakuje tlenu.
Wtedy powstają różne produkty.
Oprócz dwutlenku węgla i wody mogą powstać: tlenek węgla (CO) i węgiel (C), czyli sadza.
Tlenek węgla jest bardzo trujący!
Sadza to ten czarny osad, który widzisz np. na dnie garnka, który stał na ogniu.
Metanol – czym jest?
Metanol (CH3OH) to alkohol.
Wygląda jak woda, ale jest silnie trujący.
Stosowany jest w przemyśle jako rozpuszczalnik i do produkcji innych substancji chemicznych.
Nigdy go nie pij!
Równanie spalania całkowitego metanolu
Najpierw zobaczmy, jak wygląda spalanie całkowite metanolu:
2CH3OH + 3O2 → 2CO2 + 4H2O
W tym przypadku, przy dostatecznej ilości tlenu, metanol spala się do dwutlenku węgla i wody.
Równanie spalania niecałkowitego metanolu – przykłady
Teraz przejdźmy do spalania niecałkowitego.
Ponieważ tlenu jest za mało, reakcja może przebiegać na różne sposoby, tworząc różne produkty.
Przykład 1: Powstawanie tlenku węgla
Możemy napisać równanie reakcji, w której powstaje tlenek węgla (CO):
2CH3OH + 2O2 → 2CO + 4H2O
W tej reakcji zamiast dwutlenku węgla powstaje trujący tlenek węgla.
Przykład 2: Powstawanie węgla (sadzy)
Możemy też napisać równanie, w którym powstaje węgiel (C), czyli sadza:
CH3OH + O2 → C + 2H2O + H2
W tej reakcji powstaje sadza, woda i wodór. Ta reakcja jest bardzo uproszczona i w praktyce powstają też inne produkty.
Przykład 3: Mieszanka produktów
Często spalanie niecałkowite daje mieszaninę różnych produktów:
2CH3OH + 2.5O2 → CO2 + CO + 4H2O
W tym przypadku powstaje zarówno dwutlenek węgla, jak i tlenek węgla.
Dlaczego to ważne?
Zrozumienie spalania niecałkowitego jest ważne z kilku powodów.
Po pierwsze, pozwala zrozumieć, dlaczego niektóre pożary są bardziej niebezpieczne niż inne.
Po drugie, pomaga kontrolować procesy spalania w silnikach i elektrowniach, aby zminimalizować emisję szkodliwych substancji.
Po trzecie, uświadamia zagrożenia związane z nieprawidłowym spalaniem, np. w piecach grzewczych.
Podsumowanie
Spalanie metanolu może być całkowite lub niecałkowite.
Spalanie całkowite daje dwutlenek węgla i wodę.
Spalanie niecałkowite daje tlenek węgla, węgiel (sadzę) i wodę, a także inne związki.
Pamiętaj: tlenek węgla jest trujący!
Zawsze dbaj o odpowiednią wentylację, jeśli używasz urządzeń spalających paliwa.
Dzięki temu unikniesz niebezpieczeństwa zatrucia tlenkiem węgla.
Mam nadzieję, że teraz rozumiesz proces spalania niecałkowitego metanolu.
Powodzenia w dalszej nauce chemii!