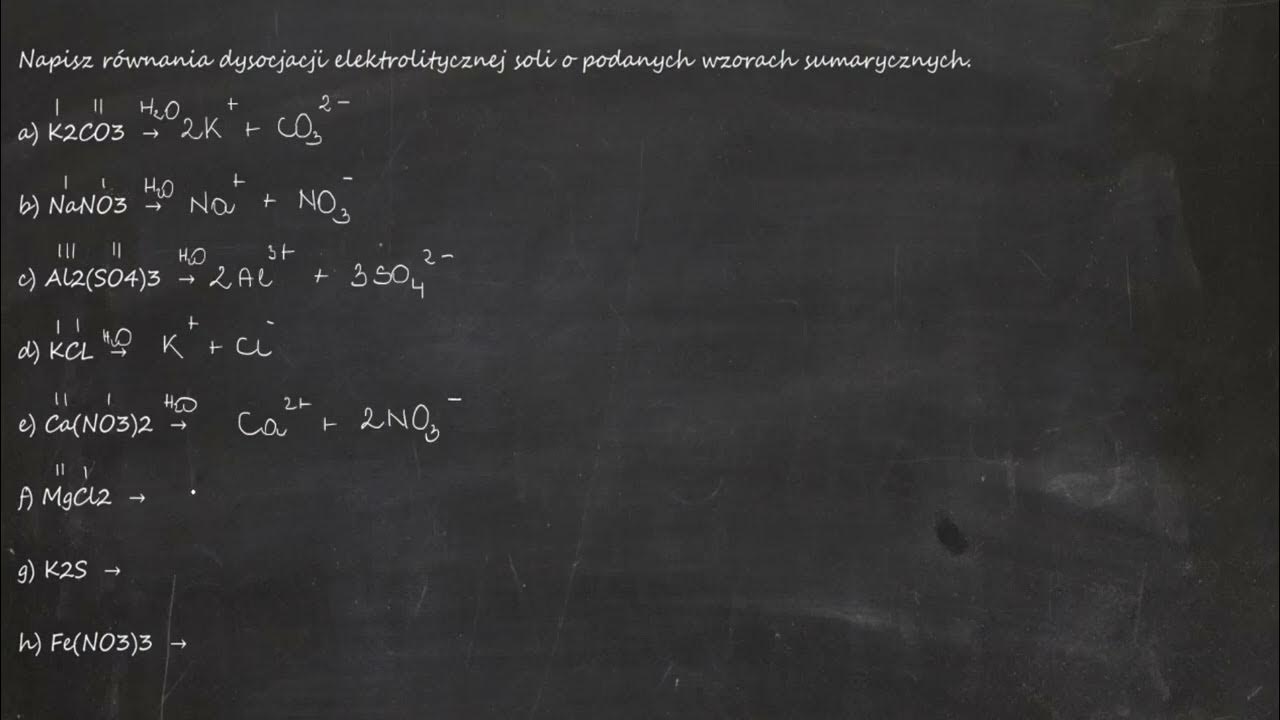Zajmiemy się teraz nazywaniem soli na podstawie ich wzorów sumarycznych. Jest to ważna umiejętność w chemii. Pozwala nam na komunikację na temat związków chemicznych. Zrozumienie nomenklatury chemicznej jest kluczowe.
Co to są Sole?
Sole to związki chemiczne. Powstają w wyniku reakcji kwasów z zasadami. Proces ten nazywamy reakcją zobojętniania. W reakcji tej kwas i zasada reagują ze sobą tworząc sól i wodę.
Sole składają się z kationu i anionu. Kation pochodzi od zasady. Anion pochodzi od kwasu. Łączą się one ze sobą tworząc sieć krystaliczną. Sieć ta charakteryzuje sól.
Nazewnictwo Soli: Zasady Ogólne
Nazwa soli składa się z dwóch części. Pierwsza część to nazwa anionu pochodzącego od kwasu. Druga część to nazwa kationu pochodzącego od zasady. Ważne jest, aby znać nazwy kwasów i zasad, aby móc poprawnie nazywać sole.
Nazwę anionu tworzy się od nazwy kwasu. Kwas beztlenowy tworzy anion o końcówce "-ek". Kwas tlenowy tworzy anion o końcówce "-an". Przykładowo, kwas solny (HCl) tworzy anion chlorkowy (Cl-), a kwas siarkowy(VI) (H2SO4) tworzy anion siarczanowy(VI) (SO42-).
Przykłady Nazywania Soli
Spójrzmy na kilka przykładów nazw soli. To pozwoli nam lepiej zrozumieć te zasady. Zaczniemy od prostych przykładów, a potem przejdziemy do bardziej złożonych.
NaCl
Wzór sumaryczny to NaCl. Kationem jest Na+, czyli sód. Anionem jest Cl-, pochodzący od kwasu solnego (HCl), czyli chlorek. Nazwa soli to chlorek sodu. Jest to pospolita sól kuchenna.
CaCO3
Wzór sumaryczny to CaCO3. Kationem jest Ca2+, czyli wapń. Anionem jest CO32-, pochodzący od kwasu węglowego (H2CO3), czyli węglan. Nazwa soli to węglan wapnia. Jest to główny składnik kamienia wapiennego.
K2SO4
Wzór sumaryczny to K2SO4. Kationem jest K+, czyli potas. Anionem jest SO42-, pochodzący od kwasu siarkowego(VI) (H2SO4), czyli siarczan(VI). Nazwa soli to siarczan(VI) potasu. Jest wykorzystywany jako nawóz.
FeCl2
Wzór sumaryczny to FeCl2. Kationem jest Fe2+, czyli żelazo(II). Anionem jest Cl-, pochodzący od kwasu solnego (HCl), czyli chlorek. Nazwa soli to chlorek żelaza(II). Ważne jest określenie stopnia utlenienia żelaza, ponieważ żelazo może występować na różnych stopniach utlenienia.
FeCl3
Wzór sumaryczny to FeCl3. Kationem jest Fe3+, czyli żelazo(III). Anionem jest Cl-, pochodzący od kwasu solnego (HCl), czyli chlorek. Nazwa soli to chlorek żelaza(III). Zauważ, że różni się od chlorku żelaza(II) tylko stopniem utlenienia żelaza.
Soli Kwaśne i Zasadowe
Oprócz soli obojętnych, istnieją sole kwaśne i zasadowe. Powstają one, gdy nie wszystkie atomy wodoru w kwasie zostaną zastąpione przez kation metalu. Lub gdy nie wszystkie grupy hydroksylowe w zasadzie zostaną zastąpione przez anion kwasowy.
W nazewnictwie soli kwaśnych używamy przedrostka "wodoro-" lub "diwodoro-". Oznacza on, ile atomów wodoru pozostało w anionie. Na przykład, NaHCO3 to wodorowęglan sodu.
W nazewnictwie soli zasadowych używamy przedrostka "hydroksy-". Oznacza on obecność grupy hydroksylowej (OH-) w kationie. Na przykład, Cu(OH)Cl to hydroksychlorek miedzi(II).
Soli Uwodnione (Hydraty)
Niektóre sole krystalizują z wodą. Woda jest wbudowana w strukturę krystaliczną soli. Takie sole nazywamy hydratami. W nazwie hydratu podajemy liczbę cząsteczek wody na jedną cząsteczkę soli.
Używamy przedrostków greckich: mono-, di-, tri-, tetra-, penta-, heksa-, hepta-, okta-, nona-, deka-. Oznaczają one odpowiednio: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 cząsteczek wody. Na przykład, CuSO4·5H2O to pentahydrat siarczanu(VI) miedzi(II).
Podsumowanie
Nazywanie soli jest kluczowe dla komunikacji chemicznej. Zaczynamy od określenia kationu i anionu. Określamy ich pochodzenie od zasady i kwasu. Następnie tworzymy nazwę soli zgodnie z ustalonymi zasadami. Pamiętamy o uwzględnianiu stopni utlenienia metali. Zwracamy uwagę na obecność wody krystalizacyjnej. Teraz potrafisz nazwać sole o podanych wzorach sumarycznych. Ćwicz dalej, aby utrwalić tę wiedzę.