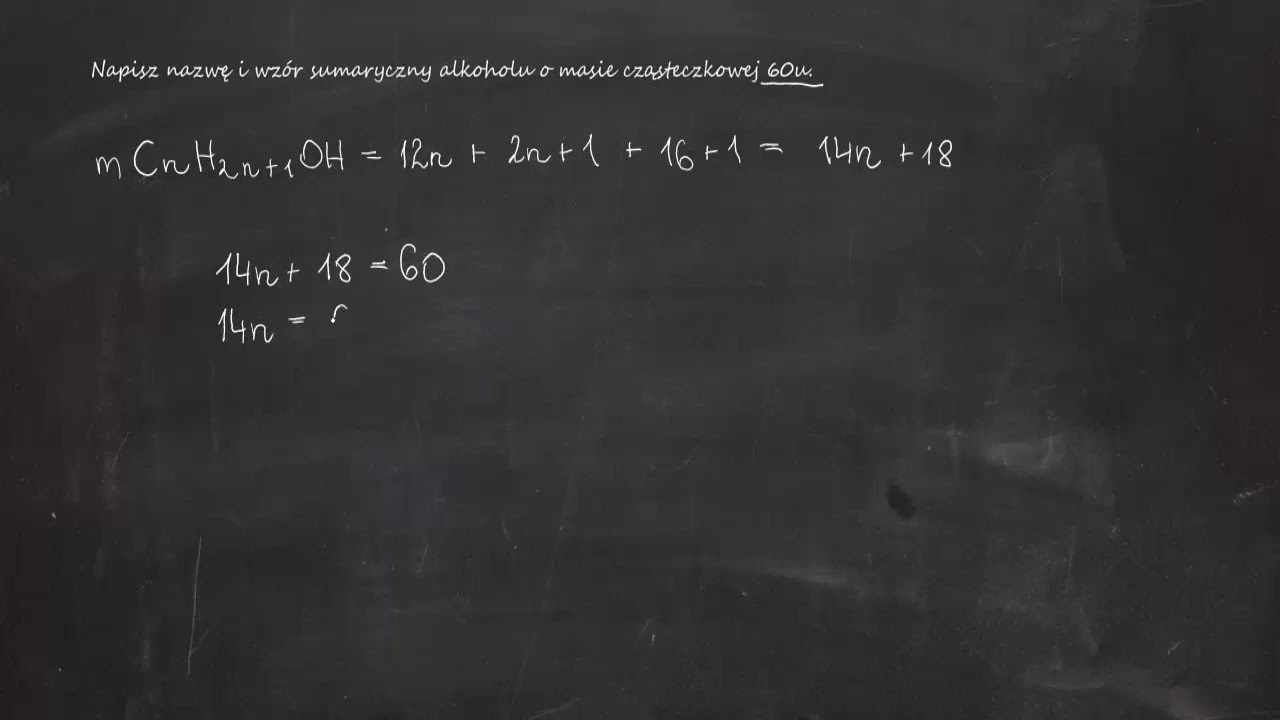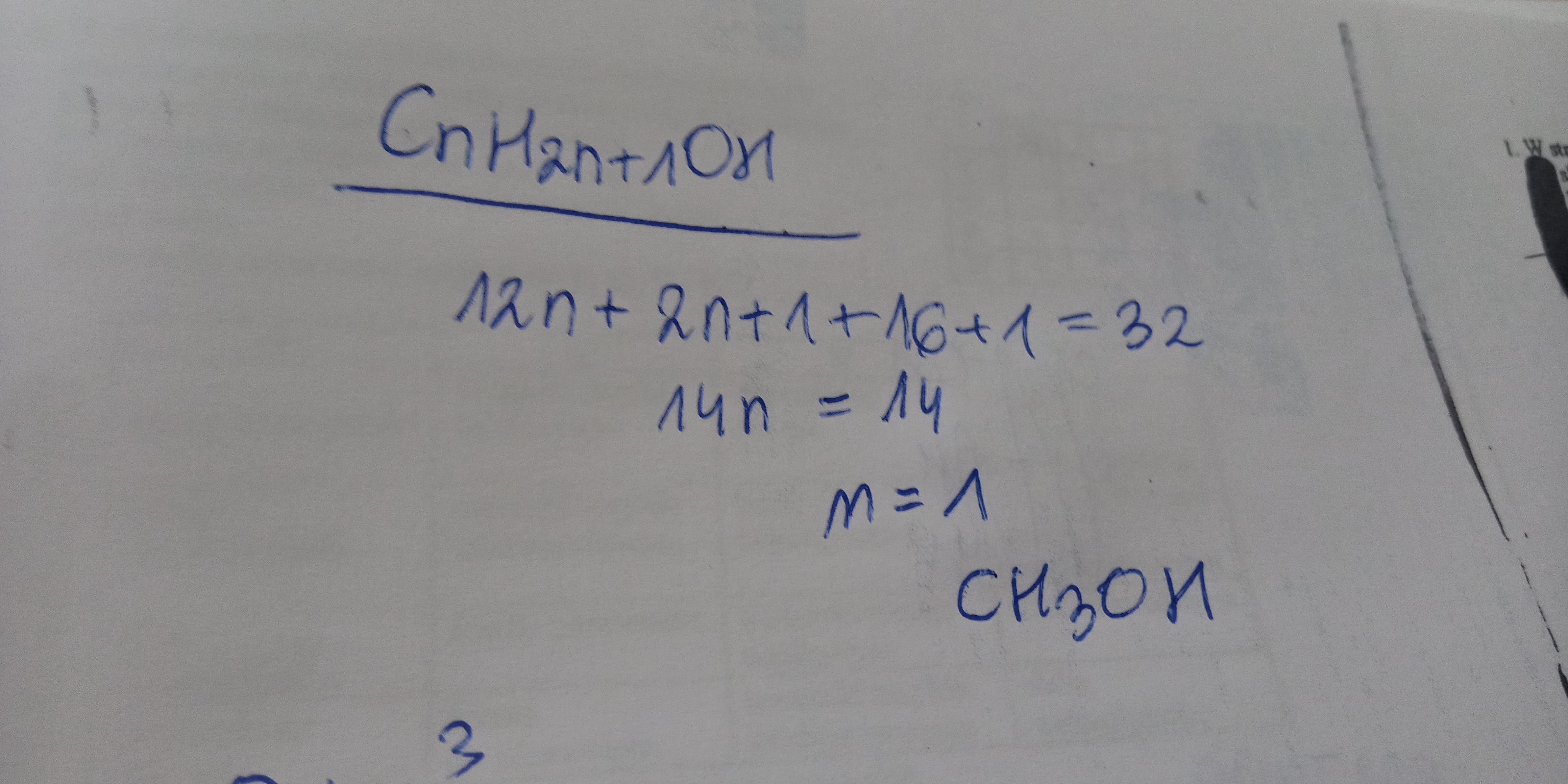Drodzy nauczyciele chemii!
Porozmawiajmy o zadaniu, które często pojawia się na lekcjach: znalezienie alkoholu o danej masie cząsteczkowej.
Dziś skupimy się na alkoholu o masie 60 u.
Identyfikacja Alkoholu o Masie Cząsteczkowej 60 u
Szukamy alkoholu, który ma masę cząsteczkową równą 60 u. Jak to zrobić?
Zacznijmy od ogólnego wzoru alkoholi: CnH2n+1OH.
Musimy znaleźć 'n' - liczbę atomów węgla.
Masa molowa węgla (C) wynosi około 12 u.
Masa molowa wodoru (H) wynosi około 1 u.
Masa molowa tlenu (O) wynosi około 16 u.
Podstawiamy do równania: 12n + 1(2n+1) + 16 + 1 = 60.
Upraszczamy: 12n + 2n + 1 + 17 = 60.
Dalej: 14n + 18 = 60.
Odejmujemy 18 od obu stron: 14n = 42.
Dzielimy przez 14: n = 3.
Zatem mamy 3 atomy węgla.
Podstawiamy n = 3 do wzoru CnH2n+1OH.
Otrzymujemy: C3H7OH.
To jest propanol.
Wzór sumaryczny to C3H8O.
Nazwa Alkoholu
Nazwa tego alkoholu to propanol.
Istnieją dwa izomery propanolu: propan-1-ol i propan-2-ol (izopropanol).
Wskazówki dla Nauczycieli
Wykorzystajcie modele atomów, aby wizualizować budowę cząsteczek.
Podzielcie uczniów na grupy i dajcie im zadanie znalezienia różnych alkoholi o zadanej masie cząsteczkowej.
Użyjcie interaktywnych symulacji online do budowy cząsteczek.
Zastosujcie analogie z życia codziennego, np. porównajcie budowę cząsteczek do budowy domów z klocków.
Zorganizujcie konkurs, w którym uczniowie będą musieli jak najszybciej zidentyfikować alkohol na podstawie masy cząsteczkowej.
Typowe Błędy i Nieporozumienia
Uczniowie często mylą wzór sumaryczny ze wzorem strukturalnym.
Często zapominają o dodaniu atomu tlenu i wodoru z grupy -OH.
Mają trudności z obliczaniem masy cząsteczkowej.
Nie rozróżniają izomerów.
Myślą, że tylko jeden alkohol może mieć masę 60u.
Jak Zapobiegać Błędom
Wyjaśnijcie różnicę między wzorem sumarycznym a strukturalnym.
Przeprowadźcie ćwiczenia z obliczania masy cząsteczkowej.
Wytłumaczcie pojęcie izomerii na prostych przykładach.
Podkreślcie, że grupa -OH jest integralną częścią alkoholu.
Zwróćcie uwagę, że izomery mają ten sam wzór sumaryczny, ale różną strukturę.
Jak Uatrakcyjnić Naukę o Alkoholach
Przeprowadźcie doświadczenie z identyfikacją alkoholi na podstawie ich właściwości fizycznych (np. zapach, rozpuszczalność).
Omówcie zastosowanie alkoholi w życiu codziennym (np. etanol w napojach alkoholowych, izopropanol w środkach dezynfekujących).
Zaproście gościa - chemika, który opowie o swojej pracy z alkoholami.
Pokażcie film dokumentalny o produkcji alkoholi.
Stwórzcie grę planszową, w której uczniowie będą musieli identyfikować alkohole i budować ich modele.
Wykorzystajcie humor i anegdoty, aby rozluźnić atmosferę na lekcji.
Zorganizujcie quiz z nagrodami dla najlepszych uczniów.
Używajcie memów chemicznych, aby zainteresować uczniów tematem.
Pamiętajcie, że nauka chemii może być fascynująca! Kluczem jest ciekawe przedstawienie materiału i aktywne zaangażowanie uczniów.
Powodzenia!