Zajmiemy się teraz kwasem fosforowym(V), substancją o wzorze sumarycznym H3PO4. Jest to jeden z najważniejszych kwasów w chemii, zarówno w laboratoriach, jak i w przemyśle. Poznamy jego właściwości, zastosowania oraz sposób powstawania.
Definicja i Wzór Sumaryczny
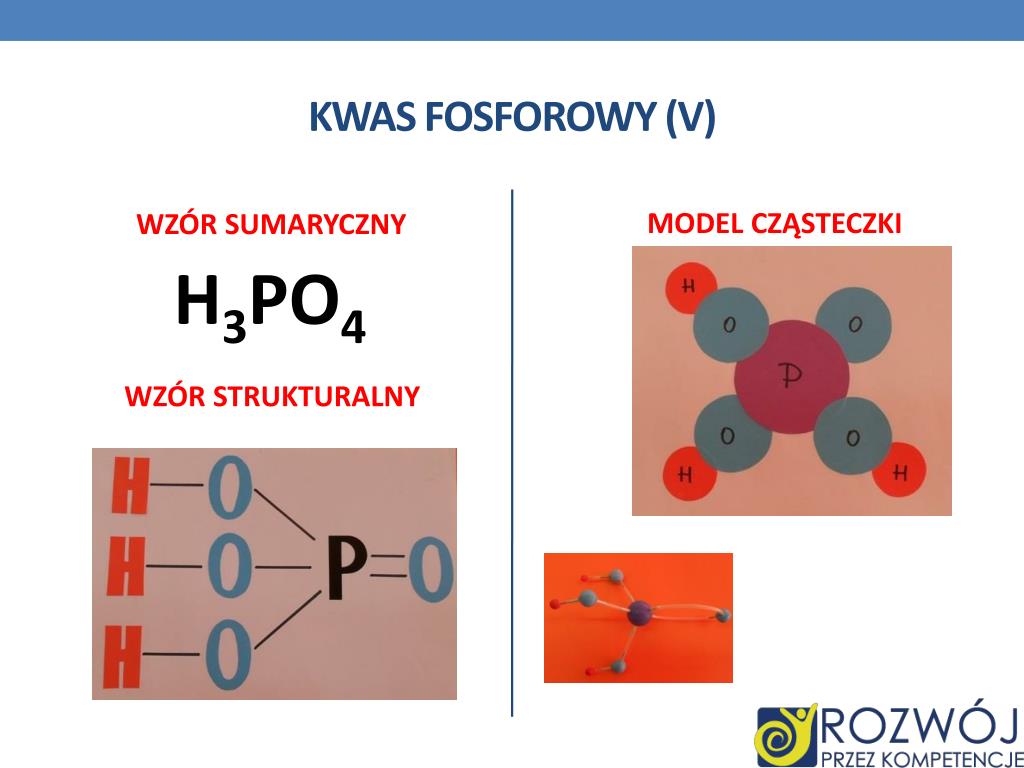
Kwas fosforowy(V), znany również jako kwas ortofosforowy, to nieorganiczny kwas. Jego wzór sumaryczny to H3PO4. Wzór ten mówi nam, że każda cząsteczka kwasu fosforowego(V) składa się z trzech atomów wodoru (H), jednego atomu fosforu (P) i czterech atomów tlenu (O).
Warto zaznaczyć, że istnieje kilka kwasów fosforowych, ale najczęściej, gdy mówimy o "kwasie fosforowym", mamy na myśli właśnie kwas ortofosforowy (H3PO4). Inne kwasy fosforowe, takie jak kwas metafosforowy czy kwas pirofosforowy, mają inne wzory i właściwości.
Właściwości Fizyczne i Chemiczne
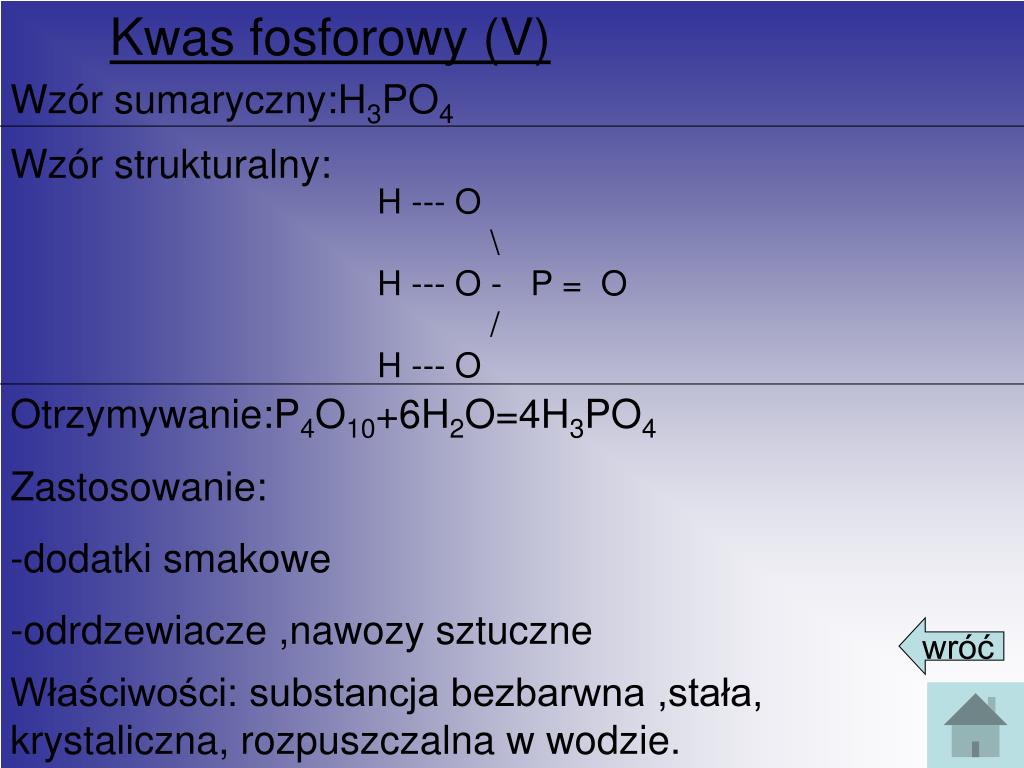
Kwas fosforowy(V) jest bezbarwną, bezwonną cieczą lub ciałem stałym (w zależności od stężenia i temperatury). Czysty kwas ortofosforowy jest substancją krystaliczną, ale zazwyczaj występuje w postaci roztworu wodnego o różnym stężeniu. Roztwory kwasu fosforowego(V) są lepkie.
Kwas fosforowy(V) jest kwasem trójprotonowym, co oznacza, że może oddawać trzy protony (jony wodorowe H+) w reakcjach z zasadami. Stopień dysocjacji zależy od pH roztworu. Dysocjacja zachodzi stopniowo, a każdy kolejny proton odrywa się trudniej niż poprzedni.
Kwas fosforowy(V) jest stosunkowo słabym kwasem nieorganicznym. Oznacza to, że w roztworze wodnym dysocjuje tylko częściowo. Jego siła zależy od stężenia.
Otrzymywanie Kwasu Fosforowego(V)
Istnieją dwa główne sposoby otrzymywania kwasu fosforowego(V): metoda termiczna i metoda mokra. Metoda termiczna polega na spalaniu fosforu w powietrzu, a następnie rozpuszczeniu powstałego tlenku fosforu(V) (P4O10) w wodzie. Metoda mokra polega na działaniu kwasem siarkowym na fosforyty lub apatyty.
Reakcja spalania fosforu: P4 + 5O2 → P4O10. Następnie tlenek fosforu(V) reaguje z wodą: P4O10 + 6H2O → 4H3PO4. Proces termiczny daje czystszy produkt, ale jest droższy.
Metoda mokra, choć tańsza, daje kwas fosforowy(V) zanieczyszczony różnymi substancjami, takimi jak związki fluoru i siarczany. Przed użyciem w niektórych zastosowaniach, kwas ten musi być oczyszczony.
Zastosowania Kwasu Fosforowego(V)
Kwas fosforowy(V) ma bardzo szerokie zastosowanie w różnych dziedzinach. Jest używany w przemyśle nawozowym do produkcji nawozów fosforowych, takich jak superfosfat i fosforan amonu. Nawozy te są niezbędne dla wzrostu roślin.
W przemyśle spożywczym kwas fosforowy(V) jest stosowany jako regulator kwasowości w napojach (np. cola), dżemach i serach. Jest również dodawany do żywności jako konserwant. Oznacza się go symbolem E338.
Kwas fosforowy(V) znajduje również zastosowanie w przemyśle farmaceutycznym, do produkcji leków i suplementów diety. Jest również stosowany w stomatologii, jako składnik materiałów do wypełnień zębów oraz w ortodoncji. Dodatkowo, jest używany jako odrdzewiacz i środek czyszczący do metalu, ponieważ reaguje z rdzą tworząc fosforany żelaza.
Ponadto, kwas fosforowy(V) jest wykorzystywany w laboratoriach chemicznych jako odczynnik w różnych reakcjach i analizach. Jest również używany w produkcji detergentów i środków czyszczących. Jego wszechstronność czyni go niezwykle ważnym związkiem chemicznym.
Przykłady Zastosowań
- Produkcja nawozów sztucznych (np. superfosfat prosty i potrójny)
- Regulator kwasowości w napojach typu cola
- Odrdzewiacz do metalu
- Składnik płynów do lutowania
- Produkcja detergentów
- Produkcja leków
Bezpieczeństwo
Należy pamiętać, że kwas fosforowy(V), szczególnie w stężonych roztworach, jest substancją żrącą. Może powodować oparzenia skóry, oczu i dróg oddechowych. Podczas pracy z kwasem fosforowym(V) należy stosować odpowiednie środki ochrony osobistej, takie jak rękawice, okulary ochronne i fartuch.
W przypadku kontaktu kwasu fosforowego(V) ze skórą lub oczami, należy natychmiast przemyć te miejsca dużą ilością wody. W razie połknięcia należy niezwłocznie skontaktować się z lekarzem.
Przechowywanie kwasu fosforowego(V) powinno odbywać się w szczelnie zamkniętych pojemnikach, w chłodnym i suchym miejscu, z dala od substancji reagujących z kwasami. Należy unikać kontaktu z metalami, które mogą korodować w kontakcie z kwasem.