Drodzy Nauczyciele,
Przygotowałem dla Was krótki przewodnik po kilku związkom chemicznym. Mam nadzieję, że pomoże Wam to w pracy z uczniami. Omówimy KMnO4, NH3, MnO2, N2, KOH i H2O. Zaczynajmy!
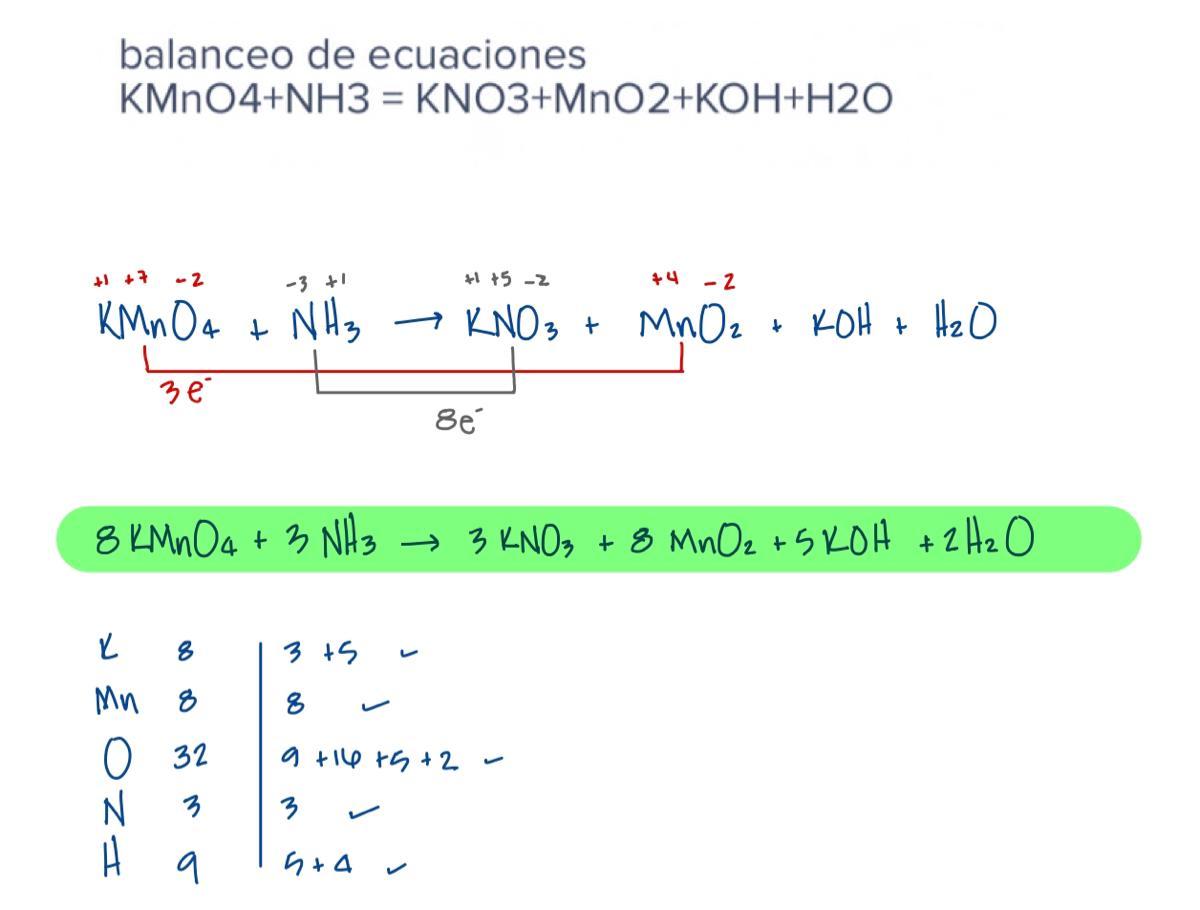
Nadmanganian potasu (KMnO4)
KMnO4 to silny utleniacz. Ma charakterystyczny fioletowy kolor. Często używany w laboratoriach chemicznych.
Warto pokazać uczniom doświadczenie z odbarwianiem KMnO4. Można użyć do tego roztworu kwasu askorbinowego (witaminy C). To wizualnie atrakcyjne i pokazuje właściwości utleniające. Pamiętajcie o zachowaniu środków ostrożności.
Częstym błędem jest mylenie KMnO4 z innymi związkami. Wyjaśnijcie, że jego fioletowa barwa jest unikalna. Podkreślcie jego rolę jako utleniacza w reakcjach chemicznych.
Amoniak (NH3)
NH3 to gaz o charakterystycznym, ostrym zapachu. Jest bezbarwny. Rozpuszcza się dobrze w wodzie.
Możecie omówić z uczniami jego rolę w przemyśle nawozowym. Wyjaśnijcie, że jest ważnym składnikiem nawozów sztucznych. Można też wspomnieć o procesie Habera-Boscha, który jest kluczowy dla produkcji amoniaku na skalę przemysłową.
Uczniowie często mylą amoniak z jonem amonowym (NH4+). Wyjaśnijcie różnicę między nimi. NH3 to cząsteczka, a NH4+ to jon powstający w wyniku przyłączenia protonu.
Tlenek manganu(IV) (MnO2)
MnO2 to czarny proszek. Jest nierozpuszczalny w wodzie. Działa jako katalizator.
Można pokazać uczniom doświadczenie z rozkładem nadtlenku wodoru (H2O2) z użyciem MnO2 jako katalizatora. To wizualnie efektowne. Wyjaśnia rolę katalizatorów w przyspieszaniu reakcji chemicznych. Pamiętajcie, że reakcja może być gwałtowna.
Często uczniowie zapominają o roli MnO2 jako katalizatora. Podkreślcie, że przyspiesza reakcję, ale sam w niej nie zużywa. Wyjaśnijcie, że reakcja rozkładu H2O2 zachodzi wolniej bez katalizatora.
Azot cząsteczkowy (N2)
N2 to główny składnik powietrza. Jest bezbarwny i bezwonny. Bardzo stabilny.
Porozmawiajcie z uczniami o znaczeniu azotu w atmosferze. Wyjaśnijcie, dlaczego jest tak ważny dla życia na Ziemi. Można też wspomnieć o cyklu azotowym.
Uczniowie mogą myśleć, że N2 jest obojętny chemicznie i nie bierze udziału w reakcjach. Wyjaśnijcie, że choć jest bardzo stabilny, to w odpowiednich warunkach może reagować (np. w procesie Habera-Boscha). Podkreślcie siłę wiązania potrójnego w cząsteczce azotu.
Wodorotlenek potasu (KOH)
KOH to mocna zasada. Jest biały. Rozpuszcza się w wodzie.
Możecie pokazać uczniom, jak KOH reaguje z kwasami. To ilustruje reakcję zobojętniania. Pamiętajcie o zachowaniu środków ostrożności, ponieważ reakcja może być egzotermiczna.
Uczniowie mogą mylić KOH z innymi zasadami, np. NaOH. Wyjaśnijcie różnice w ich właściwościach i zastosowaniach. Podkreślcie, że obie zasady są silne i żrące.
Woda (H2O)
H2O to podstawowy związek chemiczny. Niezbędna dla życia. Ma unikalne właściwości.
Omówcie z uczniami właściwości wody, takie jak wysokie ciepło właściwe, napięcie powierzchniowe i zdolność do rozpuszczania wielu substancji. Wyjaśnijcie, dlaczego woda jest nazywana "uniwersalnym rozpuszczalnikiem". Można pokazać doświadczenie z meniskiem w naczyniu.
Uczniowie często nie doceniają roli wody w procesach chemicznych i biologicznych. Podkreślcie jej znaczenie dla życia na Ziemi. Wyjaśnijcie, że woda uczestniczy w wielu reakcjach chemicznych, np. w fotosyntezie. Wyjaśnijcie pojęcie wiązania wodorowego.
Dodatkowe wskazówki
Używajcie modeli cząsteczek. To pomaga uczniom zrozumieć strukturę związków. Angażujcie uczniów w dyskusje. Zachęcajcie do zadawania pytań.
Wykorzystujcie prezentacje multimedialne. Pokazujcie filmy edukacyjne. Używajcie interaktywnych symulacji. Dzięki temu nauka będzie bardziej atrakcyjna.
Pamiętajcie o powtarzaniu materiału. Regularne powtórki utrwalają wiedzę. Stosujcie różne metody oceniania. Sprawdzajcie, czy uczniowie rozumieją materiał.
Mam nadzieję, że te wskazówki będą pomocne. Życzę Wam owocnej pracy z uczniami.
Z poważaniem,
Nauczyciel Chemii.