Hej! Zastanawiasz się, czym jest ta cała konfiguracja elektronowa? Spokojnie, zaraz wszystko stanie się jasne!
Co to w ogóle jest?
Wyobraź sobie, że atom to taki budynek mieszkalny. W samym centrum mamy jądro, czyli powiedzmy, administrację budynku. A wokół niego, na różnych piętrach, mieszkają elektrony – to jak lokatorzy.
Konfiguracja elektronowa to nic innego jak opis tego, gdzie w tym budynku mieszkają poszczególni lokatorzy. Mówi nam, na którym piętrze i w którym pokoju (dokładniej, orbitalu) znajduje się każdy elektron.
Myśl o tym jak o adresie! Każdy elektron ma swój własny, unikalny adres w atomie.
Poziomy energetyczne – czyli piętra
Te "piętra" w naszym atomowym budynku to poziomy energetyczne, oznaczane liczbami 1, 2, 3 itd. Im wyższa liczba, tym wyższe piętro i tym dalej od jądra. Na przykład, poziom 1 jest najbliżej jądra, a poziom 2 jest od niego dalszy.
Pomyśl o tym jak o odległości od administracji budynku. Im bliżej, tym łatwiej coś załatwić, ale i ciasniej.
Podpowłoki – czyli pokoje
Każde "piętro" (poziom energetyczny) ma kilka "pokoi" (podpowłok). Oznaczamy je literami: s, p, d, f.
Podpowłoka s ma tylko jeden pokój. Podpowłoka p ma trzy pokoje. Podpowłoka d ma pięć pokoi. Podpowłoka f ma aż siedem pokoi!
Wyobraź sobie, że na pierwszym piętrze (n=1) jest tylko jeden typ mieszkania – kawalerka (podpowłoka s). Na drugim piętrze (n=2) są już kawalerki (s) i mieszkania trzypokojowe (p).
Orbitale – czyli konkretne miejsca w pokojach
Każdy z tych "pokoi" (orbitali) może pomieścić maksymalnie dwa elektrony. Elektrony, żeby się nie pokłócić, muszą mieć przeciwne "spiny" – wyobraź sobie, że jeden kręci się w prawo, a drugi w lewo.
Analogia do naszego budynku: w każdym pokoju może mieszkać maksymalnie dwóch lokatorów, którzy się wzajemnie tolerują.
Zapis konfiguracji elektronowej
Konfigurację elektronową zapisujemy w prosty sposób. Najpierw piszemy numer poziomu (piętro), potem literę podpowłoki (typ pokoju), a na końcu w indeksie górnym – liczbę elektronów, które się w tej podpowłoce znajdują (ilu lokatorów mieszka w tym typie mieszkania na danym piętrze).
Na przykład: 1s2 oznacza, że na pierwszym poziomie energetycznym (piętrze) w podpowłoce s (kawalerce) znajdują się 2 elektrony (dwóch lokatorów).
Kolejny przykład: 2p4 oznacza, że na drugim poziomie energetycznym (piętrze) w podpowłoce p (mieszkaniu trzypokojowym) znajdują się 4 elektrony (czterech lokatorów).
Kolejność zapełniania orbitali
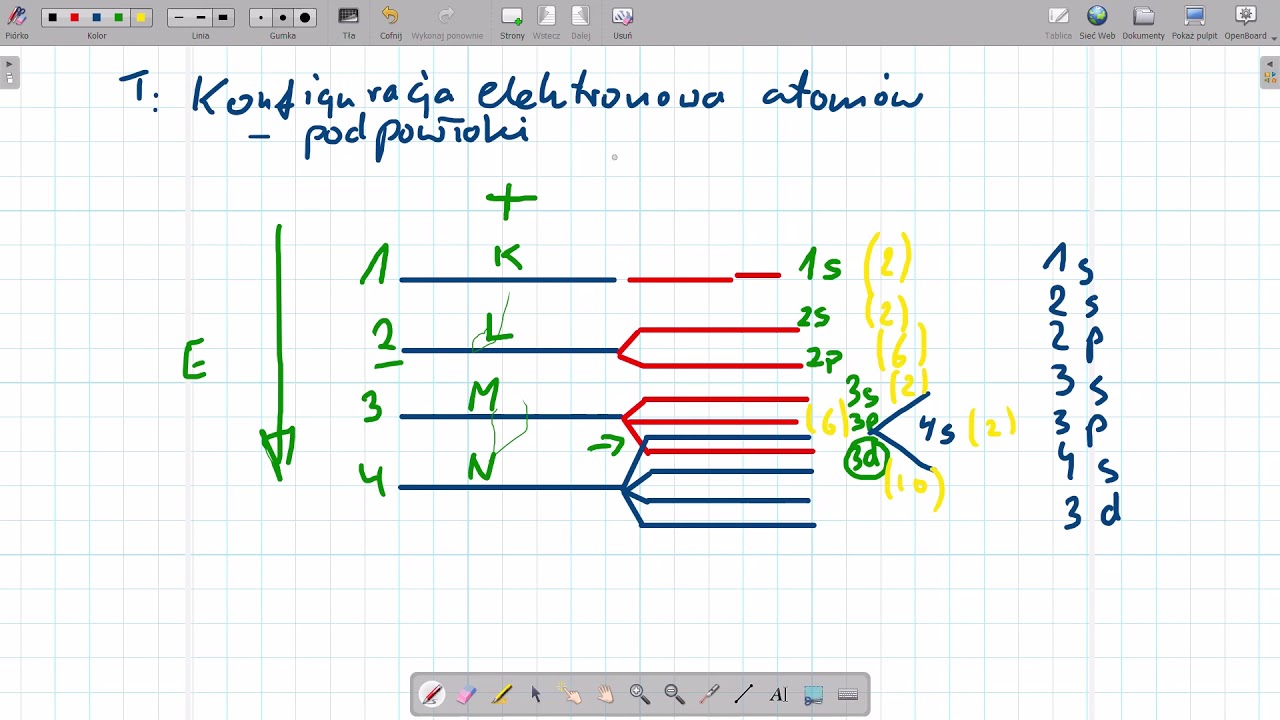
Elektrony zapełniają orbitale według pewnej kolejności. Najpierw zapełniane są te o najniższej energii. Można to zapamiętać korzystając z diagramu, który wygląda jak ścięte schody.
Mnemotechnicznie: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p...
Zapamiętaj: elektrony są leniwe i wybierają najniższe piętra (najniższe energie) dopóki nie są one zajęte!
Przykłady konfiguracji elektronowych
Zobaczmy kilka przykładów, żeby to lepiej zrozumieć:
* Wodór (H): Ma tylko jeden elektron. Jego konfiguracja elektronowa to 1s1. To tak, jakby na pierwszym piętrze (n=1) w kawalerce (s) mieszkał jeden lokator. * Hel (He): Ma dwa elektrony. Jego konfiguracja to 1s2. Pierwsze piętro i kawalerka są w pełni zajęte! * Lit (Li): Ma trzy elektrony. Jego konfiguracja to 1s22s1. Dwa elektrony mieszkają na pierwszym piętrze w kawalerce, a trzeci wprowadza się na drugie piętro, również do kawalerki. * Tlen (O): Ma osiem elektronów. Jego konfiguracja to 1s22s22p4. Dwa elektrony na pierwszym piętrze w kawalerce, dwa na drugim piętrze w kawalerce, i cztery na drugim piętrze w mieszkaniu trzypokojowym.Dlaczego to jest ważne?
Znajomość konfiguracji elektronowej jest super ważna, bo pozwala przewidzieć właściwości chemiczne danego pierwiastka. To tak, jakby znać profile mieszkańców danego budynku – możesz przewidzieć, czy będą hałaśliwi, czy spokojni!
Elektrony na ostatniej powłoce (najwyższym piętrze) – nazywane elektronami walencyjnymi – decydują o tym, jak atom będzie reagował z innymi atomami, czyli jakie wiązania będzie tworzył.
Na przykład, atomy z podobną liczbą elektronów walencyjnych mają podobne właściwości chemiczne. Wszystko zależy od tego, kto z kim chce mieszkać!
Mam nadzieję, że teraz konfiguracja elektronowa wydaje się mniej straszna. Pamiętaj o naszym budynku z lokatorami i wszystko stanie się jasne! Powodzenia!